08.02.2024

Лучевая терапия в самостоятельном варианте или в сочетании с одновременной/последовательной химиотерапией (химиолучевая терапия, ХЛТ) заняла крепкие позиции в лечении местнораспространенных форм немелкоклеточного рака легкого (НМРЛ).
Ключевой работой нынешнего десятилетия стало исследование PACIFIC, предложившее пациентам с местнораспространенным раком легкого альтернативу хирургическому вмешательству в виде конкурентной ХЛТ с последующей консолидацией дурвалумабом. Высокая эффективность этого подхода мотивировала более детальное изучение различных вариантов проведения ХЛТ, что привело к появлению ряда важных проспективных работ, о которых мы хотели бы сегодня поговорить.
В первую очередь стоит коротко упомянуть опубликованные в конце 2022 года обновленные результаты исследования PACIFIC, включившего 713 пациентов с III стадией заболевания [1]. Было показано, что проведение иммунотерапии дурвалумабом на протяжении одного года (1 раз в 2 недели, 10 мг/кг) после ХЛТ по радикальной программе (СОД 60-66 Гр и 2-3 курсов химиотерапии на основе препаратов платины) обеспечивает улучшение 5-летней общей выживаемости (ОВ) до 42,9% по сравнению 33,4% в группе ХЛТ+плацебо, а медиана выживаемости в группах составляет 47,5 и 29,1 мес. соответственно (ОР 0,72; 95% ДИ 0,59-0,89; рис.1). Проведенный post-hoc анализ показал, что главным предиктором высокой эффективности консолидирующей иммунотерапии являлась положительная экспрессия PD-L1>1% (ОР 0,61), а в группе негативной экспрессии, напротив, отмечалась тенденция к снижению общей выживаемости (рис.2).
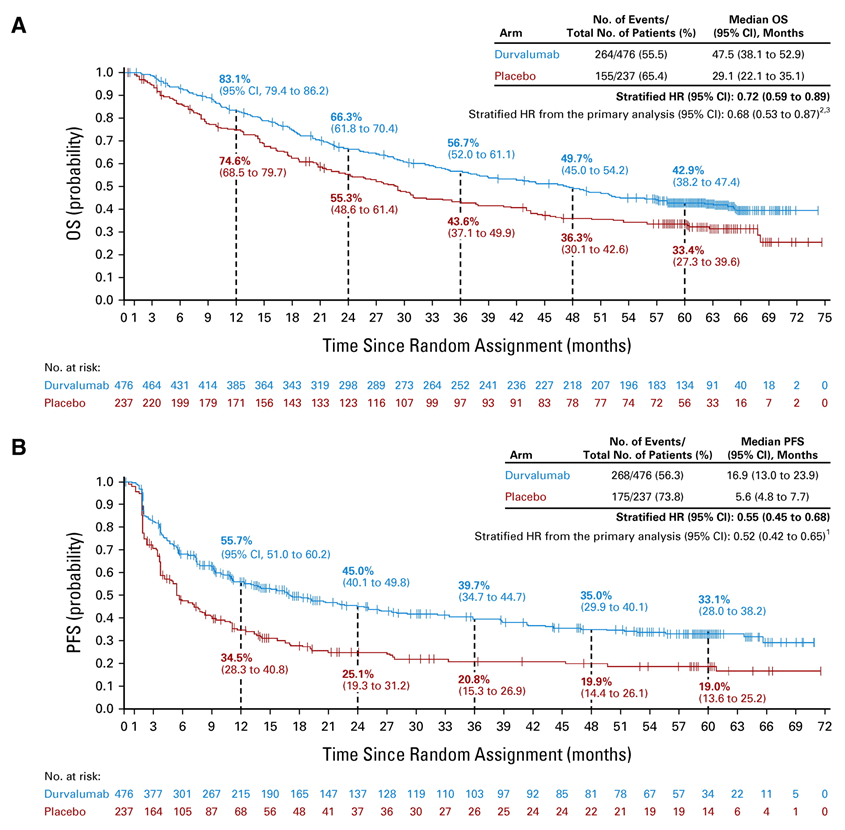
Рисунок 1. Пятилетняя общая и безрецидивная выживаемость по данным PACIFIC.
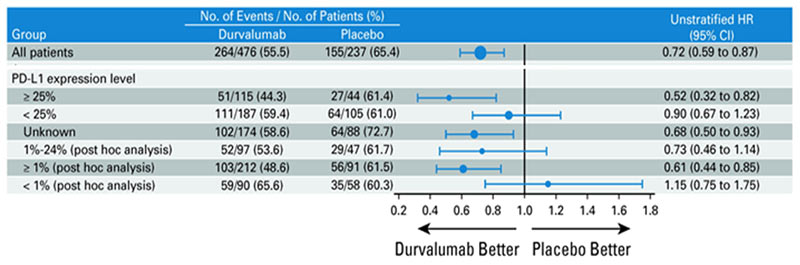
Рисунок 2. Влияние PD-L экспрессии на эффективность консолидирующей терапии дурвалумабом.
Доказанная эффективность подобного подхода не только предложила новую лечебную опцию, но и мотивировала дальнейшее ее изучение. Так, в 2022 году были опубликованы результаты небольшого исследования II фазы PACIFIC-6, целью которого стало изучение переносимости дурвалумаба в дозе 1500 мг 1 раз в 4 недели (до 24 курсов) и влияния последовательной химиолучевой терапии c подобным дозовым режимом на эффективность лечения [2]. Авторы показали, что токсичность 3-4 ст. развилась у 18,8% пациентов, а у 21,4% стала причиной прекращения лечения. Для сравнения: оригинальный протокол (10 мг/кг 1 раз в 2 недели) приводил к развитию НЯ 3-4 ст. у 30,5% пациентов. Изменение дозовой интенсивности также приводило к некоторому уменьшению показателя 2-летней выживаемости без прогрессирования (ВБП) – 35,3% против 45% в исследовании PACIFIC (рис.3).
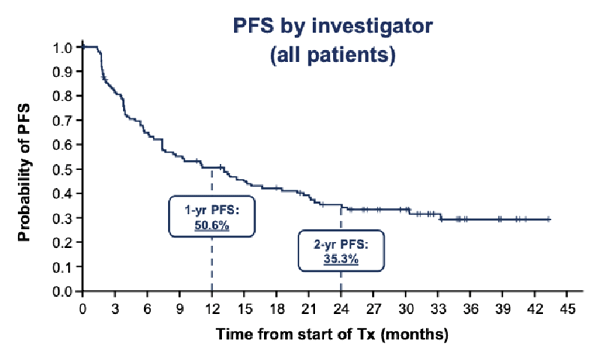
Рисунок 3. Выживаемость без прогрессирования в исследовании PACIFIC-6.
Несмотря на это, исследование показало, что пролонгация лечения является применимой опцией и может быть выбрана у ряда пациентов. Однако PACIFIC-6 подвергается аргументированной критике ввиду недостаточно четкой стратификации пациентов по возрасту и сопутствующей патологии, отсутствию подгруппового анализа по показателю экспрессии PD-L1 и, главное, меньшей медиане длительности лечения (32 недели против 40 недель в PACIFIC), что не согласуется с картиной меньшей или сопоставимой токсичности [3].
Также изучалась возможность одновременного проведения ХЛТ и иммунотерапии. Однако в конце 2023 года компания AstraZeneca сообщила о недостижении авторами исследования PACIFIC-2 первичной конечной точки, заключавшейся в улучшении показателя выживаемости без прогрессирования при проведении конкурентной ХЛТ с одновременной иммунотерапией дурвалумабом. К сожалению, детальное описание полученных негативных результатов по состоянию на февраль 2024 года опубликовано не было, что делает дальнейший анализ данной работы невозможным [4].
В декабре 2023 года были опубликованы результаты небольшого однорукавного исследования II фазы SPIRAL-RT [5]. Дизайн работы предполагал оценку 1-годичной выживаемости без прогрессирования на фоне самостоятельной ЛТ (СОД 54-66 Гр) и консолидирующей терапии дурвалумабом у пациентов с III ст. НМРЛ и противопоказаниями к проведению химиотерапии (n=33). Авторы показали, что отказ от проведения химиотерапии приводит к достоверному снижению 1-годичной ВБП до 39,1% (исторический контроль в PACIFIC – 55,7%) и общей выживаемости до 71,7% (83,1% в PACIFIC) (рис.4). Частота нежелательных явлений составила 39,4%.
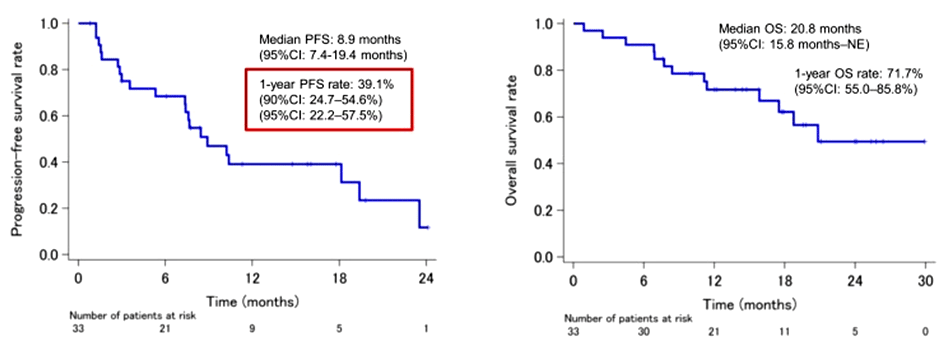
Рисунок 4. Выживаемость без прогрессирования и общая выживаемость в SPIRAL-RT.
Не меньший интерес вызывает влияние снижения дозы ионизирующего излучения на отдаленные результаты лечения. Ответить на него взялись авторы исследования DUART, предварительные данные которого были доложены на конференции ESMO 2023 в Мадриде [6]. Исследование включило 102 пациента с III cт. НМРЛ и противопоказаниями к проведению химиотерапии. Больные были рандомизированы в группы стандартной (60 Гр ± 10%) или «паллиативной» ЛТ (СОД 40-54 Гр) с последующей терапией дурвалумабом (1500 мг 1 раз в 4 недели до года). Авторы показали, что снижение суммарной очаговой дозы ассоциируется со снижением 1-годичных показателей как безрецидивной (40,2% в группе стандартной ЛТ против 29,3% в группе паллиативной ЛТ), так и общей выживаемости (67% против 56,3%) (рис.5). Тем не менее, для формулировки окончательных выводов необходимо дождаться публикации всех результатов исследования.
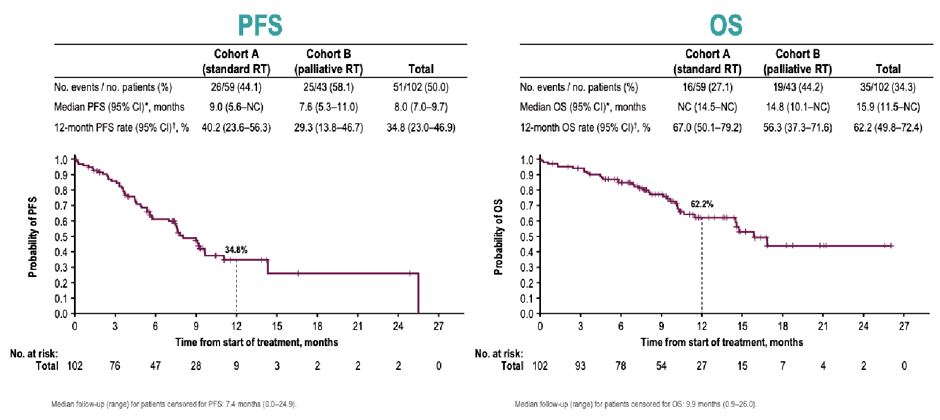
Рисунок 5. Выживаемость без прогрессирования и общая выживаемость в DUART.
Консолидация результатов приведенных исследований демонстрирует четкую корреляцию между сохранением дозовой интенсивности лучевой терапии, одномоментностью химиотерапии и эффективностью лечения (рис.6). Можно заключить, что методом выбора у неоперабельных пациентов с III стадией по-прежнему является проведение одновременной химиолучевой терапии с консолидирующей иммунотерапией дурвалумабом при наличии положительной экспрессии PD-L1. В то же время «щадящие» режимы являются хорошей опцией для тех больных, кто в силу старшего возраста или выраженности сопутствующей патологии не может претендовать на полноценное лечение по протоколу PACIFIC.

Рисунок 6. Сводная таблица исследований PACIFIC, PACIFIC-6 и DUART.
Take-home Message:
Источники: