21.10.2023

В первый день на конгрессе представлены работы, отражающие перспективы терапии раннего рака молочной железы (РМЖ).

На церемонии открытия ESMO Award for Translational Research 2023 вручена профессору Nicholas Turner (он возглавляет Центр Ральфа Лорена по исследованиям в области рака молочной железы и также является лидером группы молекулярной онкологии Центра современных исследований рака молочной железы при Институте Исследования Рака, Великобритания) за изучение роли циркулирующих опухолевых ДНК в качестве предиктора рецидива при раннем раке молочной железы; также отмечена роль профессора Turner в исследовании динамики цДНК, как метода оценки эффективности терапии при диссеминированном РМЖ.
Научная программа 1 дня включала несколько исследований, посвященных периоперационной иммунотерапии в комбинации с химиотерапией при раннем раке молочной железы, прежде всего, это KEYNOTE-522 (тройной негативный РМЖ) и CheckMate 7FL (ГР+ РМЖ) и KEYNOTE-522 (ГР+ РМЖ). Нужно отметить, что интерес к иммунотерапии при РМЖ сейчас крайне высок.
KEYNOTE-522
Представлены обновленные результаты известного и широко обсуждаемого исследования 3 фазы KEYNOTE-522, в котором изучалась целесообразность добавления пембролизумаба к химиотерапии при раннем трижды негативном РМЖ. В некоторых странах результаты данного исследования послужили причиной одобрения пембролизумаба в периоперационной терапии в рутинной клинической практике.
В работу были включены пациенты (n=1174) с ТНРМЖ с T1c N1-2 или T2-4 N0-2 и ECOG статусом 0-1, рандомизированные в две лечебные группы. Дизайн исследования представлен на рисунке 1.
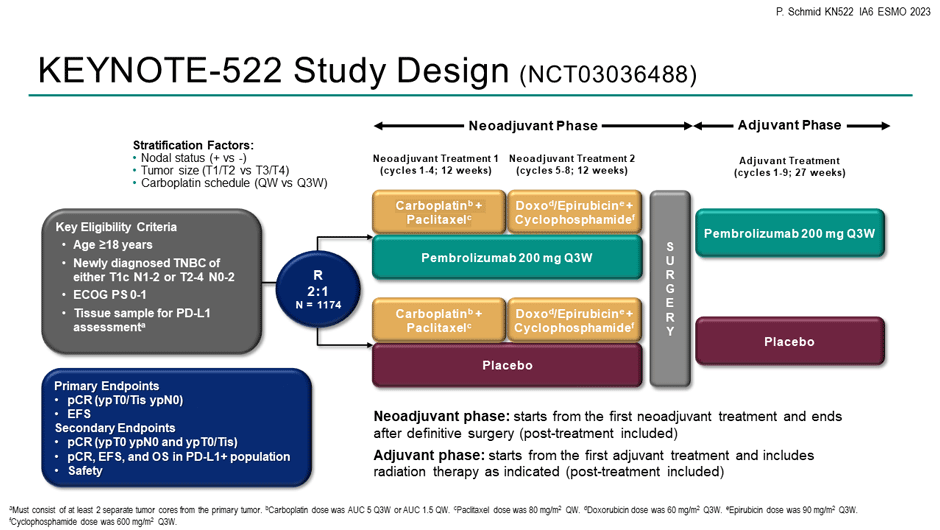
Рисунок 1. Дизайн исследования KEYNOTE-522.
У большинства пациентов в исследовании PD-L1 статус был оценен как позитивный (83,7% и 81,3%), первичная опухоль – T1/T2 (74,0% и 74,4%) и лимфатические узлы как N+ (51,7% и 51,7%). При медиане времени наблюдения в 63,1 мес. добавление пембролизумаба к химиотерапии позволило увеличить 60-месячную бессобытийную выживаемость (БСВ) с 72,3% до 81,3% (ОР 0,63; 95% ДИ 0,49-0,81) и снизить риск прогрессирования на 27% (рис.2).
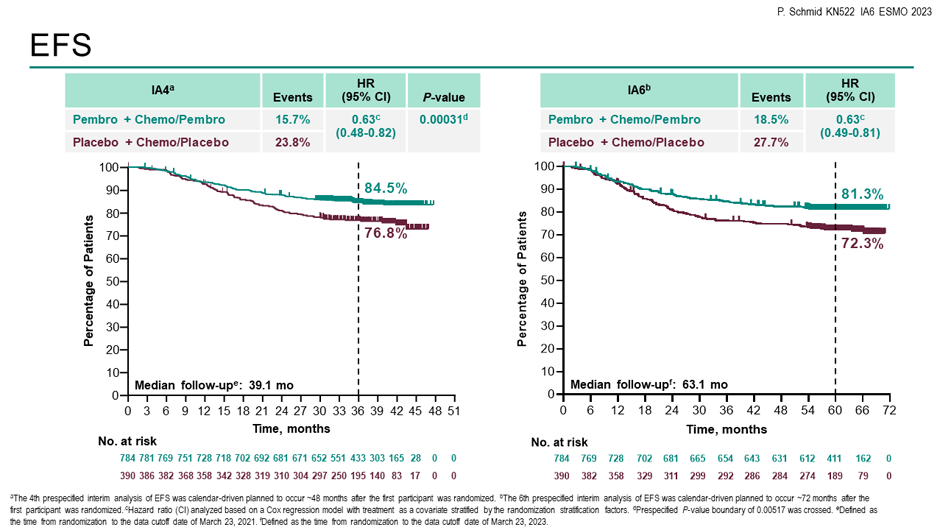
Рисунок 2. Результаты исследования KEYNOTE-522.
Интересен анализ результатов в зависимости от полного патоморфологического ответа (pCR). Так, в группе с pCR добавление пембролизумаба увеличивало 60-месячную БСВ только на 3% – с 88,2% до 92,2%, но если pCR не был достигнут, то в этой крайне неблагоприятной когорте пациентов комбинация химиотерапии с иммунотерапией позволяла увеличить этот показатель уже на 10% – с 52,3% до 62,6%.
Новое направление в периоперационной иммунотерапии РМЖ – иммунотерапия при раннем гормонозависимом РМЖ. Напомним, что частота достижения pCR при раннем рецептор-позитивном РМЖ, по данным разных авторов, варьирует от 0% до 18%.
KEYNOTE-756 – первые результаты
KEYNOTE-756 – исследование 3 фазы, основной задачей которого была оценка целесообразности добавления пембролизумаба к НАПХТ на основе антрациклинов и таксаном.
В исследование были включены больные РМЖ grade 3, начиная со стадии T1c-T2 (≥2 см) сN1-2 или T3-T4 cN0-2. Пациенты были рандомизированы в две лечебные группы 1:1:
Дизайн исследования представлен на рисунке 3.
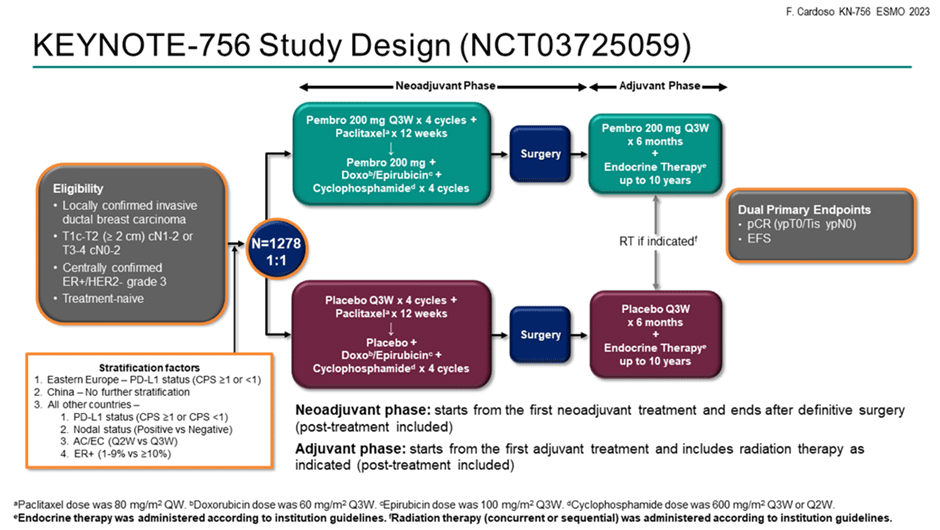
Рисунок 3. Дизайн исследования KEYNOTE-756.
Первичными конечными точками исследования были частота достижения pCR и БСВ.
У большинства пациентов, включенных в работу, зарегистрирован CPS≥1 (75,9% и 76,0%), первичная опухоль T3/T4 (36,7% и 35,8%), и лимфатические узлы оценены как метастатические в 89,8% и 90,5% случаев в 2 группах соответственно.
Добавление пембролизумаба к химиотерапии позволило увеличить частоту достижения ypT0/Tis ypN0 на 8,5% – c 15,6% до 24,3%. Fatima Cardoso особенно подчеркнула, что максимальный выигрыш от добавления иммунотерапии отмечен у больных с уровнем ЭР <10%. Нежелательные явления (НЯ) любой степени отмечены у 98,4% и 98,6% больных в лечебных группах и были преимущественно представлены алопецией (60,4% и 60,9%), тошнотой (48,3% и 50,0%), анемией (32,3% и 25,5%), слабостью (30,0% и 28,0%), диарей (27,1% и 20,2%), повышением уровней АСТ (24,9% и 22,9%) и АЛТ (21,% и 16,7%), нейтропенией (23,0% и 24,6%), астенией (21,1% и 18,1%), рвотой (20,0% и 16,8%) и полинейропатией (17,5% и 20,2%). НЯ 3 степени и выше зарегистрированы у 52,5% и 46,4% соответственно.
В группе с иммунотерапией иммуноопосредованные НЯ любой степени были преимущественно. представлены гипотиреозом (17,5%), гипертиреозом (9,0%), пневмонитом (2,8%), надпочечниковой недостаточностью (2,5%).
CheckMate 7FL
Представлены первые результаты рандомизированного исследования 3 фазы CheckMate 7FL, посвященного целесообразности добавления ниволумаба к химиотерапии (P+AC/ddAC) при раннем гормонозависимом РМЖ при T1c-T2 cN1-N2 или T3-T4 cN0-cN2.
В две лечебные группы был рандомизирован 521 больной, представлен анализ эффективности у 510 пациентов. Первичной конечной точкой исследования была частота достижения pCR в лечебных группах, вторичными – pCR при PD-L1+, а также частота достижения RCB 0/1/2/3 в зависимости от статуса PD-L1. У большинства пациентов, включенных в исследование, имелись метастазы в подмышечные лимфоузлы (80% и 79%), PD-L1+ ≥34%, а степень злокачественности опухоли оценена как grade 3 (98% и 99%).
Добавление ниволумаба к химиотерапии позволило увеличить частоту достижения pCR в ITT популяции с 13,8% до 24,5% (p=0,0021), при PD-L1≥1% комбинации с иммунотерапией привела к росту pCR с 20,2% до 44,3% (рис.4).
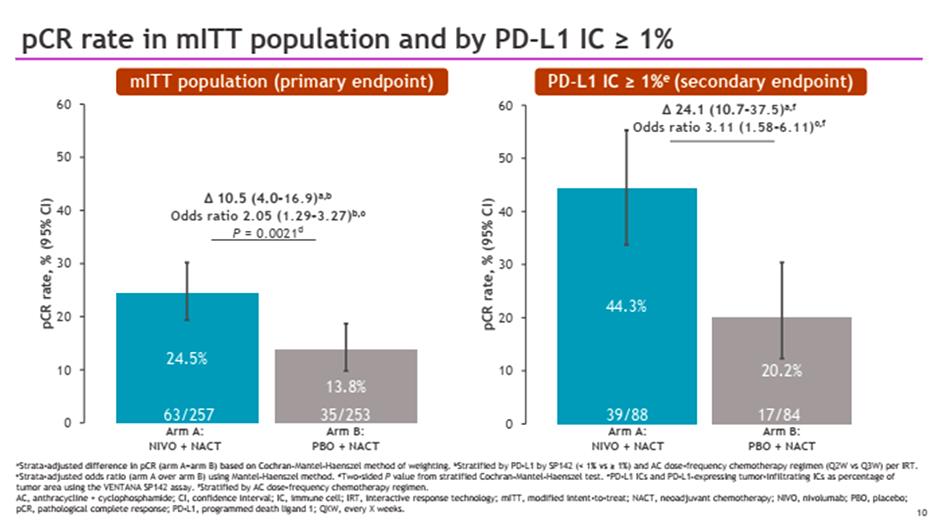
Рисунок 4. Эффективность ниволумаба в комбинации с химиотерапией при раннем ГР+ РМЖ.
Комбинация ХТ с иммунотерапией также привела к росту RCB 0-1 при PD-L1≥1% с 26,2% до 54,5% (ОР 3,49; 95% ДИ 1,82-6,69).
НЯ любой степени были зарегистрированы у 98% пациентов как в группе с ниволумабом, так и без него, причем НЯ, потребовавшие прекращения терапии, отмечены у 10% больных в группе с иммунотерапией и у 3% при назначении только химиотерапии. Зарегистрировано 2 случая смерти связанными с иммуноопосредованными НЯ.
Иммунотерапия – крайне интересная и наиболее вероятно перспективная опция при раннем РМЖ, однако эксперты осторожно относятся к представленным данным и ждут отдаленных результатов этих и будущих работ.
Источники: