10.10.2023

9-12 сентября 2023 года в Сингапуре состоялась очередная Всемирная конференция по раку легкого (World Conference on Lung Cancer), где были представлены результаты наиболее актуальных исследований, посвященных терапии рака легкого.
Опубликован проект обновления TNM при раке легкого (РЛ) для 9-го издания Классификации злокачественных опухолей
Корректировки к 9 изданию сделаны с целью улучшения прогностической ценности стадирования. Итак, новое:
FLAURA2
FLAURA2 – рандомизированное исследование III фазы, направленное на изучение эффективности осимертиниба в комбинации с химиотерапией (пеметрексед с цисплатином/карбоплатином) в первой линии лечения местнораспространенного (стадии IIIB-IIIC) или метастатического (стадия IV) немелкоклеточного рака легкого (НМРЛ) с мутацией гена EGFR.
557 пациентов были рандомизированы в две лечебные группы (1:1):
Лечение продолжалось до прогрессирования или неприемлемой токсичности.
Первичной конечной точкой исследования была медиана ВБП, оцененная центральной командой, вторичными – медиана ОВ, частота достижения контроля роста опухоли (КРО), длительность достигнутого ответа и токсичность терапии.
Средний возраст пациентов составил 61 год. Большинство больных, включенных в работу, были некурящими (67% и 65%), женщинами (61% и 62%) с ECOG статусом 1 (62% и 63%) и делецией в 19 экзоне (Del19) (61% и 60%) или заменой L858R (38% и 38%) в 21 экзоне в гене EGFR. У 42% и 40% пациентов в лечебных группах были метастазы в центральную нервную систему.
При медиане времени наблюдения в 16,5 мес. в группе осимертиниба и 19,5 мес. в группе комбинированной терапии медиана ВБП составила 19,9 и 29,4 мес. (ОР=0,62; 95% ДИ 0,48-0,80; p=0,002) соответственно, Добавление химиотерапии к осимертинибу позволило увеличить 12-месячную ВБП с 67% до 80%, 24-месячную – с 47% до 62% и статистически значимо снизить риск прогрессирования на 38%.
Добавление химиотерапии к осимертинибу позволило достигнуть частоты ОО в 83,2% против 75,5% в группе монотерапии и увеличить длительность ответа с 15,3 до 24 мес. Максимальный эффект от комбинированной терапии отмечен у пациентов с метастазами в ЦНС, добавление химиотерапии к осимертинибу увеличило медиану ВБП с 13,8 до 24,9 мес. (ОР=0,47; 95% ДИ 0,33-0,66) и статистически значимо снизило риск прогрессирования на 53%. Эффективность терапии не зависела от типа активирующей мутации гена EGFR (Ex19del vs L858R).
НЯ 3 степени и более были значимо выше в группе комбинированного лечения в сравнении с монотерапией осимертинибом: 64% и 27%, что ожидаемо.
HERTHENA-Lung01
Исследование HERTHENA-Lung01 посвящено эффективности патритумаба дерукстекана (HER3-DXd) при НМРЛ с мутацией в гене EGFR.
Патритумаб дерукстекан (HER3-DXd) представляет собой конъюгат, состоящий из моноклонального антитела (IgG1) к рецептору HER3 и ингибитора топоизомеразы I.
В исследование 2 фазы HERTHENA-Lung01 были включены больные НМРЛ с мутацией в гене EGFR, ранее получавшие ИТК и химиотерапию на основе платины. В работу также были включены пациенты с бессимптомными метастазами в головном мозге. Первоначально пациенты были рандомизированы (1:1) в две лечебные группы: первая – с фиксированной дозой HER3-DxD – 5,6 мг/кг 1 раз в 3 недели и группа с повышением дозы с 3,2 мг/кг до 4,8 мг/кг и 6,4 мг/кг в течение трех первых циклов. Однако набор во вторую группу был завершен досрочно на основании «оценки соотношения пользы и риска».
Текущие результаты отражают эффективность терапии у 225 пациентов, получавших HER3-DxD в фиксированной дозе 5,6 мг/кг 1 раз в 3 недели. Более чем у половины пациентов, включенных в исследование, были метастазы в центральную нервную систему (51%), и в среднем больные ранее получили три линии терапии (92,9% – ТКИ третьего поколения, около 40% – иммунотерапию и всем пациентам была проведена химиотерапия на основе препаратов платины).
При медиане времени наблюдения в 18,9 мес. в общей группе пациентов медиана ВБП достигла 5,5 мес. при медиане ОВ в 11,9 мес. Частота достижения объективного ответа (ОО) составила 29,8%, при КРО в 73,8% и медиане длительности ответа в 6,4 мес. При подгрупповом анализе ЧОО не зависела от возраста, пола, мутации в гене EGFR, наличия метастазов в головном мозге и иммунотерапии в анамнезе. Эффективность терапии также не зависела от уровня экспрессии HER3 (рис.1).
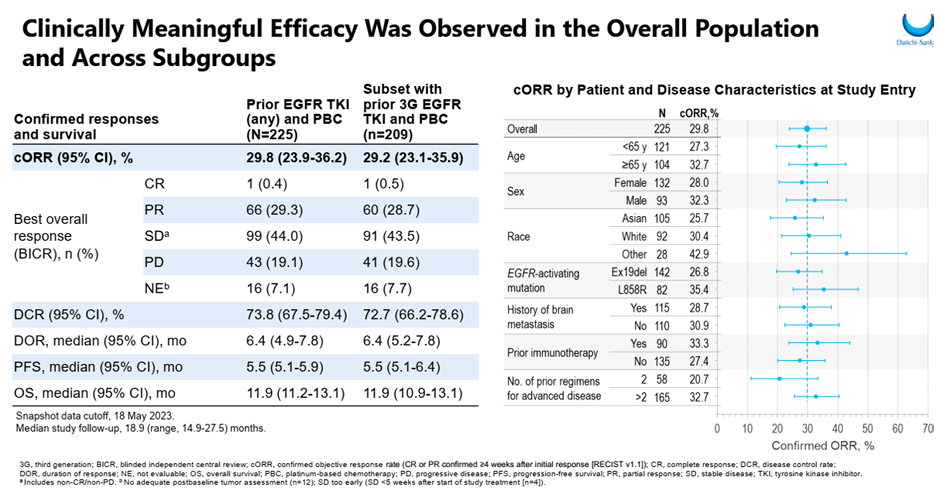
Рисунок 1. Результаты исследования HERTHENA-Lung01
(клинически значимая эффективность во всей популяции и в подгруппах).
Среди 30 пациентов с измеримыми метастазами в головной мозг у 33,3% был подтвержден ОО. В этой группе больных КРО составил 76,7%, при длительности ответа в 8,4 мес.
НЯ любой степени были зарегистрированы у 99,6% пациентов, но только в 7,1% случаев привели к прекращению терапии. НЯ 3 степени и выше, связанные с лечением, отмечены у 45,3% больных и были преимущественно представлены тромбоцитопенией (21%), нейтропенией (19%), анемией (14%), лейкопенией (10%), слабостью (6%). Пульмонит развился у 5,3% пациентов, 1 пациент погиб от интерстициальной болезни легких.
TROPION-Lung04
На конгрессе представлены первые результаты мультикогортного исследования TROPION-Lung04, посвященного изучению датопотамаба дерукстекана (Dato-DXd) в комбинации с дурвалумабом ± карбоплатин у пациентов с местнораспространенным или диссеминированным НМРЛ без активирующих мутаций с ECOG статусом 0-1. Первичная конечная точка исследования – токсичность терапии, вторичные – частота достижения ОО и КРО.
Датопотамаб дерукстекан (Dato-Dxd) представляет собой конъюгат, состоящий из моноклонального антитела (IgG1) к рецептору Trop-2 и ингибитора топоизомеразы I.
Дизайн исследования представлен на рисунке 2.
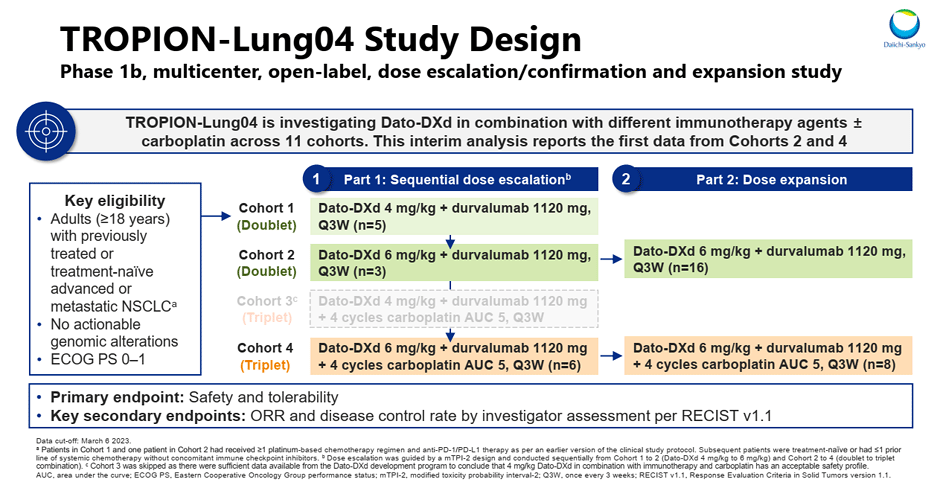
Рисунок 2. Дизайн исследования TROPION-Lung04.
Представлены промежуточные результаты второй (n=19) и четвертой (n=14) когорт:
Большинство пациентов, включенных в исследование, были мужчинами (73,7% и 64,3%) с неплоскоклеточным РЛ (73,4% и 71,4%), получавшими терапию в качестве первой линии лечения (73,7% и 92,9%). Частота ОО во 2 когорте достигла 47,4% и 71,4% – в 4 когорте.
НЯ 3 степени в первой когорте и выше были преимущественно представлены стоматитом (11%), слабостью (5%), анемией (5%), нейтропенией (5%), тошнотой (5%) и пневмонией (11%), во второй – анемией (36%), тромбоцитопенией (21%), диареей (14%), нейтропенией (14%), лейкопенией (7%) и пневмонией (7%). Гематологическая токсичность была ожидаемо значимо выше в когорте больных на химиотерапии.
DESTINY-Lung02
Представлены первые результаты исследования DESTINY-Lung02, отражающие эффективность трастузумаба дерукстекана (T-DXd) при диссеминированном неплоскоклеточном РЛ с мутацией в гене HER2.
152 больных, ранее получившие не менее 1 линии терапии, с ECOG статусом 0-1, были рандомизированы в 2 лечебные группы (2:1):
Первичной конечной точкой исследования стала ЧОО, вторичными – длительность ответа на терапию, медианы ВБП и ОВ и токсичность терапии.
Большинство пациентов, включенных в работу, были некурящими (53,9% и 58,0%), женщинами (63,7% и 68,0%), ранее получавшими anti-PD-(L)1 терапию (73,5% и 78,0%). Метастазы в ЦНС были у 34,4% и 44,0% больных в лечебных группах.
При медиане времени наблюдения в 11,5 и 11,8 мес. ЧОО в группе T-DXd 5,4 мг/кг составила 50% и 56% при дозе 6,4 мг/кг, при медиане длительности ответа в 16,8 мес. и НД. Шестимесячная ВБП в лечебных группах составила 73% при 12-месячной ВБП в 53% и 45%, а 6-месячная и 12-месячная достигли 90% и 85% и 73% и 67% соответственно.
Подробно результаты представлены на рисунке 3.
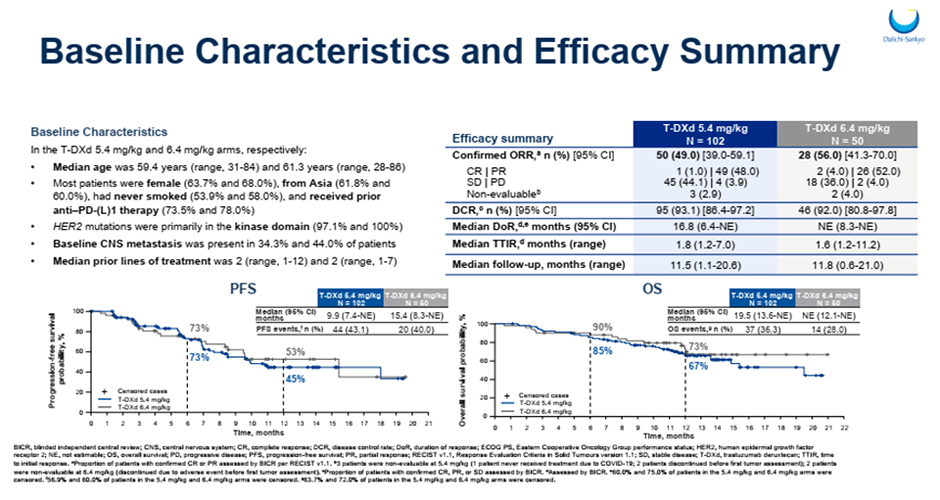
Рисунок 3. Результаты исследования DESTINY-Lung02.
При медиане длительности лечения в 7,7 мес. в группе T-DXd 5,4 мг/кг и 8,3 мес. в группе T-DXd 6,4 мг/кг НЯ любо степени были преимущественно представлены тошнотой (67,3% и 82,0%), нейтропенией (42,6% и 56,0%) и слабостью (44,6% и 50,0%). Пульмонит любой степени зафиксирован у 12,9% пациентов при дозовом режиме 5,4 мг/кг и у 28,0% больных при 6,4 мг/кг.
Исследование DS-7300 1/2 фазы, данные подгруппового анализа
Ифинатамаб дерукстекан (I-DXd) представляет собой конъюгат, состоящий из моноклонального антитела (IgG1) к рецептору B7-H3 и ингибитора топоизомеразы I.
B7-H3 – это трансмембранный гликопротеин I типа. Физиологическая роль B7-H3 остается дискуссионной и связана как с ко-стимулирующими, так и с ко-ингибирующими функциями в регуляции Т-клеточного ответа. Описывается различный уровень экспрессии B7-H3 при таких злокачественных новообразованиях, как плоскоклеточный рак слизистой оболочки полости рта (91,8%), остеосаркомы (93-100%), рак молочной железы (80,5-90,6%) и рак легкого (37,1-69,5%).
Представлены первые результаты терапии 22 пациентов с дозовым уровнем ифинатамаба дерукстекана от 3,2 мг/кг до 16,0 мг/кг.
Медиана возраста пациентов, включенных в исследование, составила 61 год. Преимущественно это были мужчины (63,6%) с ECOG статусом 1 (68,2%), ранее получавшие химиотерапию на основе платины (100%) и иммунотерапию (81,8%).
При медиане времени наблюдения в 11,7 мес. в группе пациентов, получавших I-DXd ≥6,4 мг/кг, ЧОО достигла 52,4%, при медиане времени до регистрации ОО в 1,2 мес. и медиане длительности в 5,9 мес. (рис.4).
Медиана ВБП (I-DXd≥6,4) составила 5,6 мес. (95% ДИ 3,9-8,1) при медиане ОВ в 12,2 мес. (95% ДИ 6,4-НД).
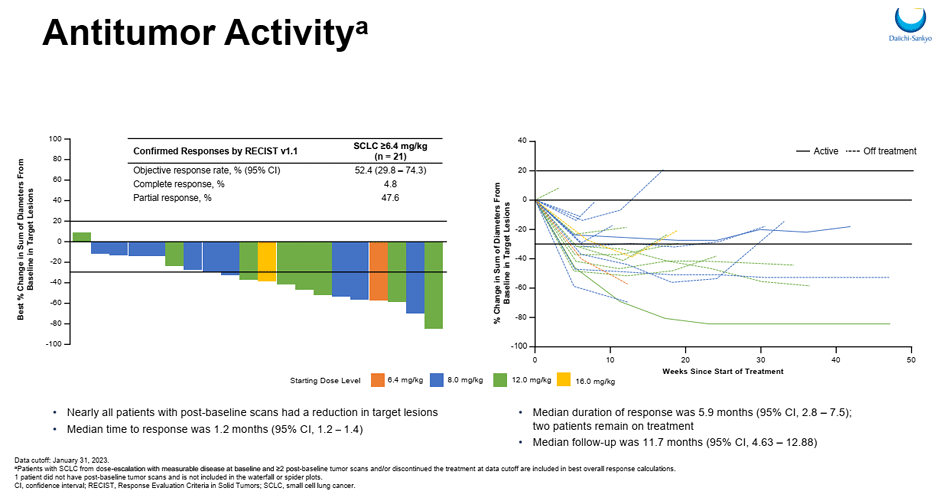
Рисунок 4. Первые результаты исследования DS-7300 1/2 фазы.
НЯ любой степени зарегистрированы у 22 больных (100%), 3 степени и выше – у 8 пациентов (36,4%) и привели к прекращению терапии в 5 случаях (22,7%). НЯ были преимущественно представлены тошнотой (59,1%), слабостью (50,0%), анемией (27,3%), рвотой (27,3%), снижением аппетита (22,7%), гипертермией (18,2%), запорами (18,2%) и диареей (13,6%).
Источники: