03.07.2023

Этот год заставил нас задуматься над уже произошедшими, продолжающимися и грядущими изменениями в лечении больных с онкогинекологической патологией. Еще совсем недавно, читая курс лекций ординаторам, я всегда говорила: неважно, какая органопринадлежность или гистологический подтип опухоли у пациентки с онкогинекологической патологией – назначая паклитаксел и карбоплатин/цисплатин в первой линии, вы никогда не ошибетесь. Это наш неизменный мировой «золотой стандарт» уже в течение последних 25-30 лет. В действительности оказалось, что стандарт пошатнуть невозможно, но он обрастает элегантными современными аксессуарами. Давайте начнем в них разбираться.
Рак яичников
Революционное исследование DUO-O затмило даже late breaking abstract на ASCO в 2023 году и является темой множественных дискуссий среди экспертного сообщества [1]. Самая главная особенность этого исследования в том, что это пока единственная работа, где иммунотерапия смогла показать позитивные результаты. Дизайн исследования, в котором участвовало 1130 пациенток, включал три рукава:
Первичной конечной точкой является медиана времени до прогрессирования (ВБП). Обратите внимание, что статистическая гипотеза носит иерархический характер, и предварительный анализ включал оценку ВБП между 1-й и 3-й когортами сперва в группе HRD-положительных больных без мутации в генах BRCA1/2, в случае позитивного результата проводился анализ в группе HRD-негативных пациенток. Предварительные данные продемонстрировали, что исследование позитивное. В группе больных с HRD+ статусом получено достоверное увеличение медианы ВБП с 23 до 37,3 мес., со снижением риска прогрессирования на 51% (HR 0,49; 95% ДИ 0,34-0,69). Предварительный анализ результатов в подгруппе больных с HRD-негативным статусом также показал статистически значимое увеличение в когорте больных, получавших тройную комбинацию: медиана ВБП составила 20,9 мес. и 17,4 мес. в группе одного бевацизумаба (HR 0,68 [0,54-0,86]). На момент окончания лечения – через 24 мес. – 40% больных не имели прогрессирования в группе бевацизумаба, олапариба, дурвалумаба, тогда как в группе одного бевацизумаба – только 24%. Подгруппа, включающая бевацизумаб с дурвалумабом, не показала достоверного преимущества против одного VEGF ингибитора. Первичное импульсивное чувство – это желание, чтобы иммунотерапия наконец-то вошла в лечение больных раком яичников и показала преимущество в группе больных без нарушений в системе репарации ДНК, а это 50% больных, которым мы не могли ничего предложить за последние 20 лет. Однако на какие нюансы стоит обратить внимание в данном исследовании. Во-первых, у нас нет адекватной контрольной группы. Например, для больных с HRD+ статусом без мутаций BRCA стандартом считается монотерапия PARP ингибитором или комбинация бевацизумаба и олапариба. Таким образом, встает вопрос: а нужно ли нам добавлять ингибитор контрольных точек иммунного ответа к этой комбинации? Ответа на этот вопрос мы пока не получим. Во-вторых, отметим, что стоимость такого дорогостоящего лечения значимо увеличивает финансовую нагрузку на систему здравоохранения всех стран мира. Поэтому необходимо четко осознавать ту пользу, которую от этого современного лечения может получить пациентка. Например, при непрямом сравнении относительных рисков прогрессирования (HR) назначение одного PARP-ингибитора нирапариба в исследовании PRIMA имеет такой же показатель, как тройная комбинация олапариба, бевацизумаба и дурвалумаба (см. таблицу 1). В-третьих, при внимательном анализе кривых на графиках стоит отметить, что при достоверном выигрыше в 3,5 мес. при использовании тройного коктейля против одного бевацизумаба не наблюдается сохраняющегося расхождения кривых после окончания терапии (см. график 1). Таким образом, продемонстрированные предварительные результаты исследования DUO-O не погружают нас в эйфорию, а оставляют нас в интригующем напряжении и заставляют ожидать финальных результатов исследования с последующим поданализом общей выживаемости (ОВ).
Таблица 1. Относительные риски прогрессирования в исследованиях по изучению иммунотерапии и PARP-ингибиторов при первичном раке яичников.
| HR | DUO-O [1] Бевацизумаб Олапариб Дурвалумаб |
PAOLA [2] Бевацизумаб Олапариб |
PRIMA [3] Нирапариб |
|---|---|---|---|
| 0,51 | 0,71 | 0,50 | |
| HRD– | 0,68 | 0,92 | 0,68 |
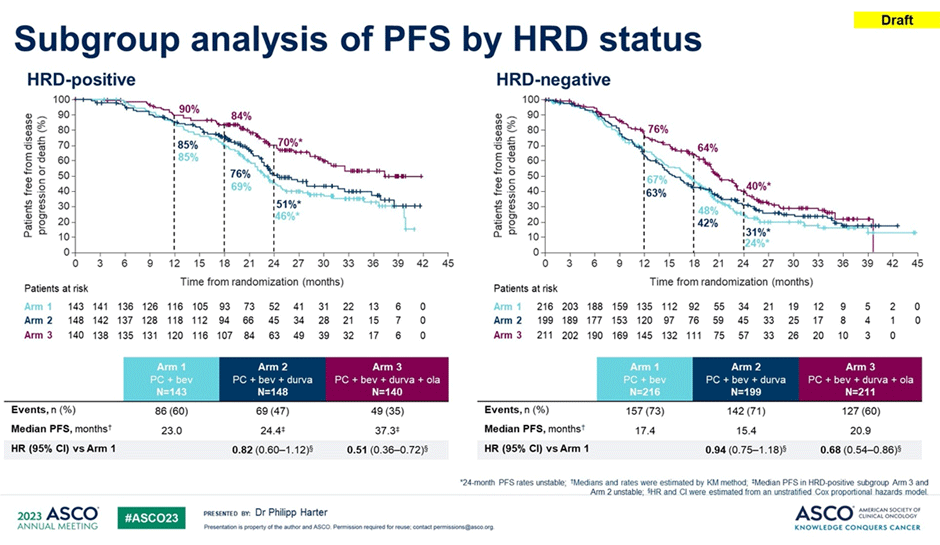
Рисунок 1. ВБП в исследовании DUO-O в зависимости от HRD статуса.
Рак шейки матки
Изменения в терапии первой линии лечения первичного метастатического или рецидивирующего рака шейки матки назрели еще 2021 году. На ASCO 2023 были озвучены финальные результаты исследования KEYNOTE 826 [4]. Напоминаю, что это рандомизированное исследование III фазы, ставившее перед собой задачу сравнить добавление пембролизумаба (35 введений) к терапии паклитакселом и препаратами платины ± бевацизумаб. В исследование было включено 617 пациенток, первичными конечными точками являлись ВБП и продолжительность жизни (ПЖ). Финальные результаты по общей выживаемости показали достоверное снижение риска смерти на 40% в подгруппе пациенток с PD-L1 СPS ≥1 при добавлении к терапии пембролизумаба. Медиана ПЖ в группе стандартной терапии составила 16,5 мес., в группе с добавлением пембролизумаба – 28,6 мес. (HR 0,60; 95% ДИ 0,49-0,74). Те больные, которым был противопоказан бевацизумаб по тем или иным причинам, также выигрывали от добавления чекпойнт ингибитора. В связи с этим FDA еще в 2021 году регистрирует пембролизумаб в первой линии лечения больных диссеминированным или рецидивирующим раком шейки матки с PD-L1 СPS ≥1. Данное показание уже внесено в рекомендации NCCN и с 2023 года планируется быть включенным в рекомендации RUSSCO. Это приводит к нескольким будущим трудностям: например, что нам назначать данным пациенткам при прогрессировании после первой линии, ведь сейчас стандартом по данным исследования II фазы является пембролизумаб. В исследовании KEYNOTE 826, если мы посмотрим внимательно на графики, отмечается сохранение расхождения кривых, и 24 месяца переживает 53% пациенток по сравнению с 39,4% в группе контроля (рис.2). Нет сомнений, что такой четверной коктейль значительно увеличивает стоимость лечения, но и достоверно увеличивает продолжительность жизни больных, сохраняя длительный контроль над болезнью у половины пациенток. Стоит отметить, что подгрупповой анализ показал: добавление пембролизумаба демонстрирует достоверное улучшение результатов выживаемости вне зависимости от назначения бевацизумаба. Однако он не показал достоверного увеличения ОВ в группе первично метастатических больных (а это 20% пациенток). Четких объяснений на этот счет нет, возможно, это связано с агрессивным течением заболевания у данной категории больных, где эффект иммунотерапии не успевает реализоваться.
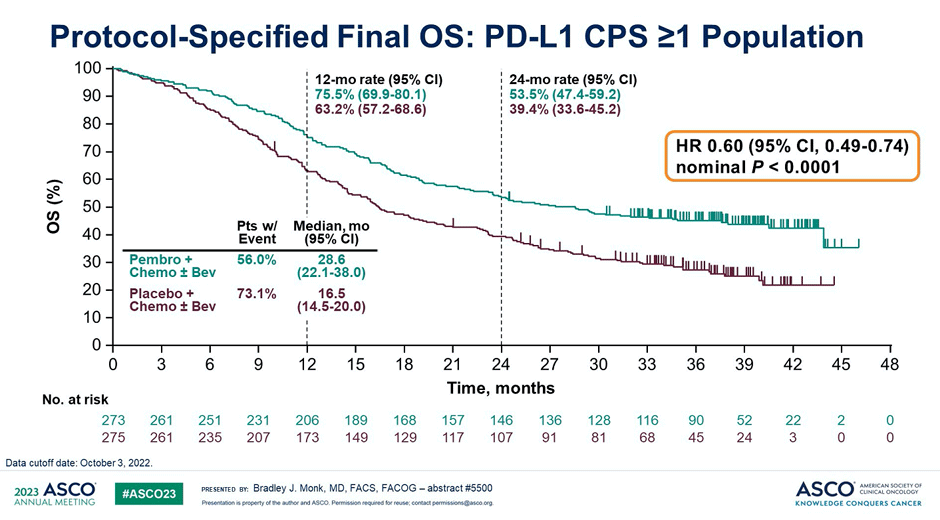
Рисунок 2. Финальные результаты ПЖ больных раком шейки матки в исследовании KEYNOTE 826.
Рак эндометрия
В первичном лечении рака эндометрия происходят аналогичные изменения. Совсем недавно мы говорили об отсутствии эффективных опций для лечения диссеминированного или рецидивирующего рака эндометрия. Наш «золотой стандарт» умеренно контролирует процесс с достижением медианы ПЖ примерно 15 месяцев. Совсем недавно произошли глобальные изменения в лечении прогрессирования после первой линии с исключением стандартной цитостатической терапии и плотным внедрением пембролизумаба для больных с дефицитом в системе репарации ДНК (dMMR) и при его отсутствии (pMMR) – усиление иммунотерапии TKI ингибитором, в данном случае комбинации пембролизумаба и ленватиниба. Научное сообщество ожидало результатов исследования LEAP-001, где изучалась вышеуказанная комбинация в качестве замены паклитакселу и карбоплатину. Однако интрига оборвалась после озвучивания двух исследований по изучению ингибиторов контрольных точек иммунного ответа в рамках первой линии лечения, что заставляет нас с марта 2023 года вести бурные дискуссии.
В марте 2023 года на конференции SGO озвучиваются результаты исследования по изучению пембролизумаба вместе с химиотерапией паклитакселом плюс карбоплатином у пациенток с метастатическим раком эндометрия и в рамках адъювантной терапии III-IV стадий в сравнении с одним «золотым стандартом» [5]. В исследовании было показано достоверное улучшение результатов при добавлении пембролизумаба у всех пациенток вне зависимости от MMR статуса. Наилучший результат получен в подгруппе больных с dMMR, в когорте пембролизумаба медиана ВБП не была достигнута, в когорте плацебо – 6 мес., 74% больных, получивших пембролизумаб, переживает 12 мес. без прогрессирования против 38% в группе контроля (HR 0,30; 95% ДИ 0,19-0,48, P<0,001). В подгруппе pMMR результаты не столь впечатляющие, но все же достоверные: в группе иммунотерапии – 13,1 мес., в группе плацебо – 8,7 мес. (HR 0,54; 95% ДИ 0,41-0,71; P<0,001).
На ASCO 2023 подтверждается значимость иммунотерапии у больных раком эндометрия в адъювантной терапии и при метастатическом процессе в качестве первой линии лечения, где подробно обсуждается исследование RUBY. В работу включены 494 пациентки с аналогичными критериями и дизайном, что и в предыдущем исследовании. Контрольный рукав включал больных, получавших «золотой стандарт» паклитакселом и карбоплатином, в экспериментальной группе пациентки получали «золотой стандарт» + достарлимаб в течение 3 лет. Анализ сравнения оценки прогрессирования исследователями и независимой командой показал идентичный результат: у пациенток с dMMR статусом медиана ВБП не достигнута при назначении достарлимаба, в группе одной химиотерапии – 7,7 мес. (HR 0,28; 95% ДИ 0,16-0,49; P<0,0001). В общей популяции, включая больных с отсутствием дефицита в системе репарации ДНК (pMMR), также наблюдается значимый положительный тренд с сохранением длительного контроля над болезнью у 36% больных: медиана ВБП в группе достарлимаба – 11,8 мес. против 7,9 мес. в группе плацебо (HR 0,64; 95% ДИ 0,50-0,80; P<0,0001). Предварительные данные по продолжительности жизни также показывают значимое преимущество от добавления достарлимаба.
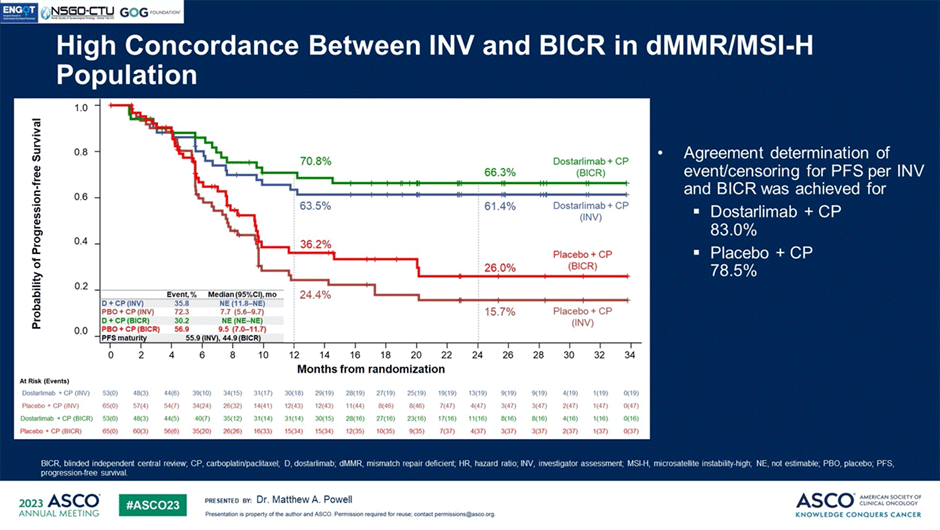
Рисунок 3. ВБП у пациенток с dMMR в исследовании RUBY в зависимости от оценки исследователями и независимой центральной командой.
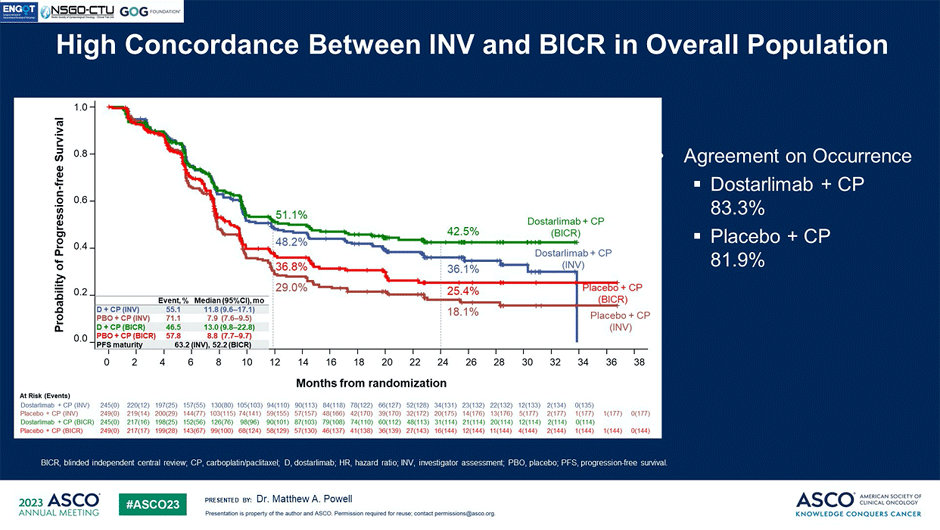
Рисунок 4. ВБП в общей популяции в исследовании RUBY в зависимости от оценки исследователями и независимой центральной командой.
Авторы провели полноценный анализ качества жизни больных, где показали, что к 7-му циклу терапии с достарлимабом достоверно улучшается качество жизни больных по сравнению с пациентками, которые получали только цитостатическую терапию [7]. К 13-му циклу терапии сохраняется та же самая тенденция, однако она становится статистически незначимой (р=0,06). Лечение с использованием иммунотерапии достоверно быстрее и чаще улучшало физической состояние пациенток, позволяло вернуться к своей повседневной деятельности, улучшало эмоциональный, когнитивный статус, сохраняло активное социальное взаимодействие.
Таким образом, добавление иммунотерапии на первом этапе лечения больных раком эндометрия стало значимым прорывом, который мы ранее никогда не наблюдали у данных пациенток. Это нашло отражение к включению комбинаций с пембролизумабом и достарлимабом. Подтверждение необходимости назначения чекпойнт ингибиторов в первой линии лечения и адъювантной терапии уже нашло свое отражение в рекомендациях NCCN 2023 года и готовится к включению в российские рекомендации. Будет оставаться открытым вопрос, что мы будем назначать пациенткам при прогрессировании на химиотерапии вместе с иммунотерапией в последующем.
Подводя итоги, хочется отметить, что мы с вами наблюдаем радостную и в то же самое время затруднительную картину, демонстрирующую новые показания для иммунотерапии, которые открываются для пациенток в онкогинекологии. Причем одновременно в трех наиболее частых встречаемых онкогинекологических патологиях. Многие мои коллеги бросились считать и сравнивать стоимость новой терапии с нашим дешевым и всем доступным «золотым стандартом» – таксанами с платиной. Даже не хочу этого делать сейчас, чтобы сильно не огорчаться, поскольку осознаю, что это увеличение стоимости лечения не в два и не в три раза. В настоящий момент наша задача совместно с государством и фармацевтическим сообществом попытаться найти взаимодействие для поиска баланса и достижения большей доступности наиболее эффективного лечения пациенткам, страдающим от злокачественных гинекологических новообразований. А в заключение хочется отметить, что «золотой стандарт» побить невозможно, его можно только дополнить.
Список литературы: