01.02.2021


C 8 по 11 декабря 2020 года состоялся 43-й Ежегодный симпозиум по раку молочной железы в Сан-Антонио (43rd Annual San Antonio Breast Cancer Symposium – SABCS). В этом году исследователями из более чем 80 стран было представлено рекордное количество абстрактов (1194 абстракта), что еще раз доказывает актуальность проведения клинических исследований, несмотря на пандемию COVID-19. Прошлый 2020 год ознаменовался прогрессом в лечении больных раком молочной железы, в США зарегистрировано 4 новых противоопухолевых препарата для лечения больных с агрессивными подтипами метастатического рака молочной железы (РМЖ).
РАННИЙ РМЖ
ER+ HER2- ранний РМЖ (рРМЖ)
Kalinsky и соавт. представили результаты одного из наиболее ожидаемых и обсуждаемых исследований SWOG S1007 RxPONDER по изучению стандартной адъювантной эндокринотерапии ± химиотерапии среди больных ER+ HER2- рРМЖ со шкалой рецидива 25 и менее с 1-3 пораженными лимфатическими узлами (ЛУ) [1]. Значение оценки риска рецидива Oncotype DX для определения больных с (ЛУ-) HR+HER2- рРМЖ, которым может не проводится химиотерапия (ХТ), было установлено в ходе исследования TAILORx в 2018 году. Однако оставалось неясным, могут ли результаты TAILORx быть экстраполированы на больных с (ЛУ+) РМЖ. В обоих клинических исследованиях для оценки риска рецидива применялся мультигенный тест Oncotype Dx.
В исследовании SWOG S1007 RxPONDER были проанализированы сведения о 5083 больных (медиана наблюдения составила 5,1 лет). В результате были зарегистрированы 447 случаев рецидива инвазивного заболевания. При первичном анализе преимущество ХТ в зависимости от шкалы рецидива не было статистически значимым (p=0,30). Однако в группе высокого риска наблюдалось снижение выживаемости без рецидива инвазивного заболевания (ОР 1,06; 95% ДИ 1,04-1,07; p<0,001). Назначение ХТ ассоциировалось с увеличением выживаемости без рецидива инвазивного заболевания (БРВ) (ОР 0,81; 95% ДИ 0,67-0,98; p=0,026). Была отмечена значимая взаимосвязь преимущества назначения ХТ и менопаузального статуса (p=0,004), которая требовала отдельного анализа. Среди постменопаузальных больных (n=3350, 67%) ОР для группы ХТ + гормонотерапия vs гормонотерапия (ГТ) не было значимым (ОР 0,97; 95% ДИ 0,78-1,22; p=0,82); 5-летняя БРВ равнялась 91,6% vs 91,9%, что свидетельствовало об отсутствии преимущества от дополнительного применения ХТ.
В группе пременопаузальных больных (n=1665, 33%), было выявлено значимое (95% ДИ 0,38-0,76; p=0,0004) преимущество от назначения дополнительной ХТ. Показатели 5-летней БРВ составили 94,2% vs 89,0% соответственно.
Таким образом, существует значимое различие в преимуществе от назначения ХТ в зависимости от риска рецидива для пременопаузальных vs постменопаузальных пациентов. Несмотря на то, что зарегистрировано лишь 8,8% случаев рецидива инвазивного заболевания и пациенты будут находиться под наблюдением в течение 15 лет, полученные данные показали, что адъювантная терапия может быть деэскалирована до применения только ГТ среди постменопаузальных больных с ЛУ+ (1-3) и индексом риска рецидива <25. Однако отмечено значимое преимущество БРВ при назначении ХТ и ГТ среди пременопаузальных больных. Также по предварительным данным наблюдается увеличение 5-летней общей выживаемости (ОВ).
Наиболее важным вопросом остается значимость ХТ в этой группе больных, так как неясно, явилось ли это преимущество следствием лишь подавления менструального цикла, т.е. супрессии овариальной функции при назначении ХТ. Дополнительное наблюдение продолжается, в дальнейшем анализ данных будет включать оценку качества жизни больных и другие вторичные точки. Также планируется анализ данных преимущества при назначении ХТ в зависимости от индукции менопаузы.
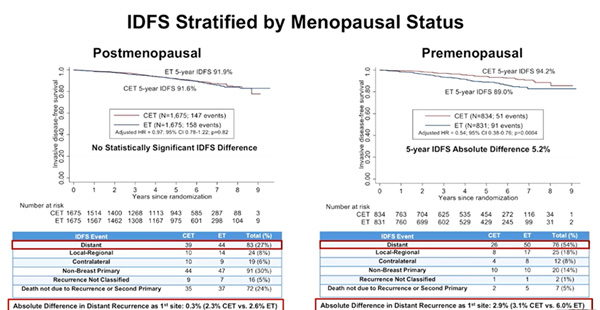
Рисунок 1. Исследование III фазы SWOG S1007 RxPONDER: стандартная адъювантная ГТ ± ХТ
среди больных (ЛУ+) ER+HER2- рРМЖ с индексом по шкале риска развития рецидива 25 и менее.
В ходе симпозиума были доложены результаты исследований МonarchE и PENELOPE-B по применению CDK4/6 ингибиторов в адъювантном режиме лечения больных HR+ HER2- рРМЖ с высоким риском развития рецидива. Предметом для дискуссий среди экспертов стала причина различий в результатах исследований.
МonarchE является исследованием III фазы, сравнивающим эффективность (БРВ) абемациклиб + ГТ vs ГТ при раннем (операбельном) РМЖ высокого риска [2].
Согласно обновленным данным, преимущество в относительных показателях выживаемости при применении абемациклиба + ГТ vs ГТ в общей группе больных составило 28,7% (ОР 0,713; 95% ДИ 0,583-0,871; p=0,0009). В группе больных абемациклиб + ГТ 2-летняя выживаемость без рецидива инвазивного заболевания достигла 92,3% против 89,3% в группе ГТ. Данные по ОВ пока не представлены. Важной вторичной конечной точкой исследования являлась оценка эффективности среди больных с высоким уровнем Ki-67 (≥20%). Абемациклиб в комбинации с ГТ продемонстрировал в данной группе больных повышение БРВ, со снижением ОР развития инвазивного заболевания на 30,9% (ОР 0,691; 95% ДИ 0,519-0,920; p=0,0111); 2-летняя выживаемость без инвазивного заболевания составила в группах абемациклиб + ГТ vs ГТ 91,6% и 87,1% соответственно. Добавление абемациклиба к ГТ также увеличивало безметастатическую выживаемость. Таким образом, при относительно короткой медиане наблюдения (приблизительно 19 месяцев) абемациклиб в сочетании с ГТ продемонстрировал клинически значимое увеличение БРВ среди больных (ЛУ+) HR+ HER- рРМЖ высокого риска, а также статистически значимое увеличение БРВ у больных с Ki-67 ≥20%.
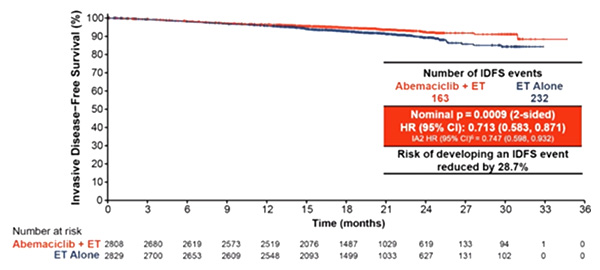
Рисунок 2. Исследование III фазы МonarchE: Эффективность абемациклиба + ГТ vs ГТ
у больных рРМЖ высокого риска.
Loibl S. и соавт. представили финальные данные по БРВ в исследовании PENELOPE-B по изучению палбоциклиба в комбинации с ГТ для лечения больных HR+ HER2- рРМЖ с резидуальным заболеванием высокого риска рецидива после неоадъювантной химиотерапии (НАХТ) [3]. В исследование III фазы PENELOPE-B включались больные, у которых не был достигнут полный патоморфологический ответ после неоадъювантной таксан-содержащей химиотерапии с высоким риском рецидива: CPS-EG (клинико-патологическая стадия + экспрессия ER+ и степень злокачественности [G]) индекс ≥3 или 2 и ypN+. В период с 02.2014 г. по 12.2017 г. 1250 больных были рандомизированы, средний возраст равнялся 49,7 (19-79) лет.
Почти у всех пациентов (96,8%) наблюдался резидуальный РМЖ: позитивный статус лимфатических узлов ypN+ выявлен среди 94,6%; G3 – 47,4%, Ki-67 >15% – среди 27,7%. Риск рецидива по CPS-EG ≥3 отмечен у 54,7% больных. Дополнительно к таргетной терапии палбоциклибом половина пациентов (50,1%) получала ингибиторы ароматазы, 49,8% – тамоксифен, 6,6% – ингибиторы ароматазы + агонисты гонадотропин-рилизинг гормона и 9,7% – тамоксифен + агонисты гонадотропин-рилизинг гормона.
Согласно результатам, при медиане наблюдения 43 месяца дополнительное назначение палбоциклиба не привело увеличению БРВ (ОР 0,93; 95% ДИ 0,74-1,17; р=0,525). Показатель безрецидивной выживаемости равнялся 88,3% в группе палбоциклиб + ГТ против 84% в группе плацебо + ГТ в течение 2 лет; 73% против 72,4% в течение 4 лет. Также не установлено различий в показателях ОВ. Докладчиком отмечена необходимость получения в будущем информации о результатах долгосрочного наблюдения при применении других CDK4/6 ингибиторов с целью оценки их эффективности. Одной из причин неудачи исследования, возможно, является отличие в определении больных группы высокого риска рецидива. В исследование включались только пациенты с резидуальным РМЖ, у которых не наблюдалось полного патоморфологического ответа (pCR). Число испытуемых в исследовании PENELOPE-B было в 4 раза меньше, чем в исследовании PALLAS и МonarchE, а также использовался как предикторный фактор рецидива CPS-EG индекс, а не стадия заболевания. Возможно, абемациклиб является более эффективным CDK4/6 ингибитором, однако это не подтверждается в исследованиях 1-й линии метастатического РМЖ, при которых отмечались схожие результаты при лечении палбоциклибом.
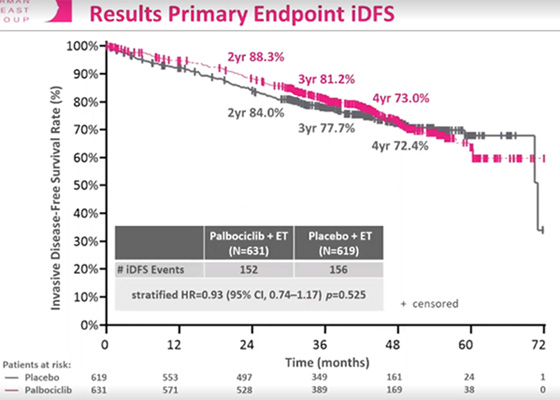
Рисунок 3. Исследование III фазы PENELOPE-B: палбоциклиб в комбинации с ГТ для лечения
пациентов с HR+ HER2- ранним (операбельным) РМЖ высокого риска рецидива после НАХТ.
РЕАБИЛИТАЦИЯ БОЛЬНЫХ РАННИМ РМЖ
В исследование биопсихосоциального подхода в реабилитации больных рРМЖ [4] были включены сведения о 228 больных, получивших комплексное лечение заболевания. Из них 114 больных были включены в проспективное исследование и на протяжении лечения подвергались реабилитационным мероприятиям в рамках биопсихосоциального подхода и 114 больных были подобраны в контрольную группу ретроспективно по методике попарного отбора. Реабилитационные мероприятия в рамках биопсихосоциальной модели улучшили показатели бессобытийной БСВ в группе больных рРМЖ: БСВ составила 18,3 мес. против 14,5 мес. в контрольной группе (ОР 0,91; 95% ДИ 0,83-0,99; p=0,0034). При многофакторном анализе ключевыми факторами, влияющими на БСВ, были НАХТ (ОР 0,79; 95% ДИ 0,69-0,94; р=0,0025), возраст (ОР 0,87; 95% ДИ 0,71-1,09; р=0,0027) и менопаузальный статус (ОР 0,85; 95% ДИ 0,84-0,95; р=0,0022). Кроме того, важно отметить, что биопсихосоциальная модель реабилитация больных рРМЖ позволяет учитывать не только биологические (генетические, анатомические, физиологические, биохимические и др.), но и психологические факторы, включающие в себя психические процессы, индивидуальные психологические особенности личности и поведения, а также социальные факторы.
МЕТАСТАТИЧЕСКИЙ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Трижды негативный метастатический РМЖ
В ходе конгресса были доложены результаты по дополнительным вторичным оценочным конечным точкам исследования KEYNOTE-355 (Rugo H. и соавт.) по изучению применения пембролизумаба в комбинации с ХТ 1-й линии терапии местно-рецидивирующего неоперабельного или метастатического трижды негативного РМЖ (ТНРМЖ) [5]. Ранее при промежуточном анализе данных было отмечено статистически значимое увеличение БПВ при применении пембролизумаба в сочетании с ХТ (наб-паклитаксел / паклитаксел / гемцитабин + карбоплатин) vs только ХТ при экспрессии PD-L1 CPS ≥10 (ОР 0,65; 95% ДИ 0,49-0,86; одностороннее значение P=0,0012, заранее оговоренный статистический критерий альфа = 0,00411). Вторичные конечные точки включали частоту объективных ответов (ОО), частоту контроля над заболеванием (полный регресс + частичный регресс + стабилизация заболевания ≥24 недель), а также длительность ответа.
Результаты по всем вторичным конечным точкам показали преимущество комбинации пембролизумаб + ХТ при наличии PD-L1 экспрессии. Частота ОО при CPS ≥10 составила 53,2% (95% ДИ 46,4-59,9%) vs 39,8% (95% ДИ 30,3-49,9%); при CPS ≥1 – 45,2% (95% ДИ 40,4-50,0%) vs 37,9% (95% ДИ 31,3-44,8%).
При подгрупповом анализе увеличение показателя ВБП в группе пембролизумаб + ХТ наблюдалось вне зависимости от комбинаторного химиотерапевтического препарата. Данные результаты вызывают особый интерес, учитывая негативные результаты в исследовании IMPASSION131, которое показало отсутствие увеличения ВБП и ОВ при назначении атезолизумаба в комбинации с еженедельным паклитакселом (возможно, по причине индуцированной иммуносупрессии, вызванной еженедельным введением дексаметазона с целью премедикации). Однако сравнение эффективности комбинаторных цитостатиков не являлось целью исследования, именно поэтому сделать объективные выводы в настоящий момент не представляется возможным. Также отмечено сравнительное снижение эффективности пембролизумаба в комбинации гемцитабин + карбоплатин, что обусловлено изначально плохим прогнозом в данной группе больных.
При CPS ≥10 выживаемость без прогрессирования в группе больных мТНРМЖ пембролизумаб + ХТ составила 9,7 мес. vs 5,6 мес. в группе плацебо + ХТ (ОР 0,65; 95% ДИ 0,49-0,86); при CPS ≥1 показатели ВБП составили 7,6 мес. vs 5,6 мес. соответственно (ОР 0,74; 95% ДИ 0,61-0,90).
На основании результатов KEYNOTE-355 в улучшении показателей выживаемости без прогрессирования FDA присвоило статус ускоренного одобрения комбинации пембролизумаб + ХТ для лечения больных с местно-рецидивирующим нерезектабельным или метастатическим ТНРМЖ с экспрессией PD-L1 (CPS ≥10). Данные по ОВ ожидаются в 2021 году.
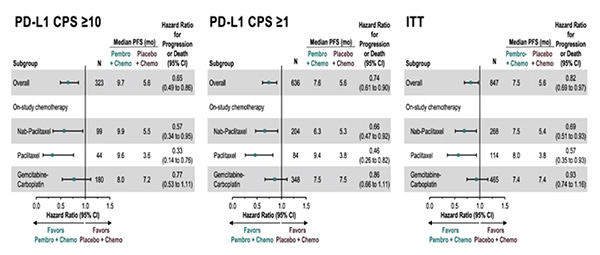
Рисунок 4. Исследование III фазы KEYNOTE-355: пембролизумаб в комбинации с химиотерапией
в 1-й линии терапии неоперабельного или метастатического ТНРМЖ.
Dent R. et al представили результаты исследования III фазы IPATunity130, анализирующего эффективность комбинации ипатасертиб + паклитаксел при мутациях в сигнальном пути PIK3CA/AKT1/PTEN в качестве 1-й линии терапии местнораспространенного или метастатического ТНРМЖ [6].
Ранее согласно результатам клинического исследования II фазы LOTUS наблюдалось увеличение показателей ВБП в группе больных ТНРМЖ с мутацией в PIK3CA/AKT1/PTEN сигнальном пути (4,9 vs 9,0 мес.; ОР 0,44; 95% ДИ 0,37-0,98).
Известно, что PIK3CA/АКТ сигнальный путь является необходимым для метаболизма, пролиферации и инвазии опухолевых клеток. Ипатасертиб – пероральный высокоспецифичный препарат, предназначенный для таргетного воздействия на все три изоформы АКТ (серин-треониновой протеинкиназы). Ипатасертиб блокирует сигнальный путь PI3K/AKT – ключевой фактор роста и пролиферации опухолевых клеток при РМЖ. Когорта А включала пациентов, у которых была обнаружена мутация в гене PIK3CA или AKT1- и/или PTEN. Пациенты не получали ранее химиотерапию по поводу распространенного ТНРМЖ.
Пациенты были рандомизированы 2:1 и получали ипатасертиб 400 мг или плацебо (день 1-21) в комбинации с паклитакселом 80 мг/м2 (Д 1, 8, 15). Отмечено отсутствие преимущества в показателях ВБП в группах пациентов, получавших ипатасертиб + паклитаксел vs плацебо + паклитаксел (7,4 vs 6,1 мес.; ОР 1,02; 95% ДИ 0,71-1,45; р=0,9237). Результаты исследования III фазы IPATunity130 отличаются от ранее полученных результатов исследований II фазы АКТ ингибиторов при ТНРМЖ: в исследовании LOTUS по изучению комбинации паклитаксел + ипатасертиб и в исследовании PAKT по изучению комбинации паклитаксел + капивасеритиб. Кроме того, необходимо выделение потенциальных биомаркеров для определения группы пациентов ТНРМЖ, которая может получить преимущество от назначения АКТ ингибиторов, в том числе и ипатасертиба.
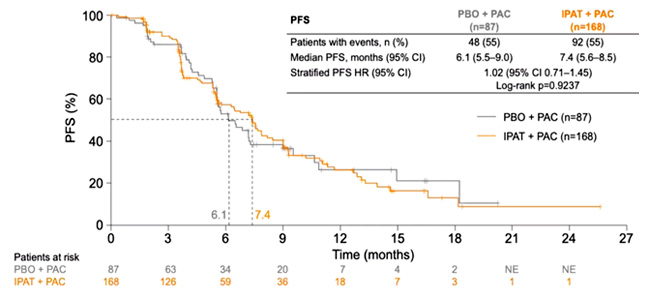
Рисунок 5. Исследование III фазы IPATunity130: ипатасертиб + паклитаксел
в 1-й линии терапии нерезектабельного или метастатического ТНРМЖ.
ER+HER2- метастатический РМЖ
O'Shaughnessy и соавт. представили результаты исследования III фазы CONTESSA по ВБП при применении тезетаксела в комбинации с редуцированной дозой капецитабина (1650 мг/м2) vs стандартная доза капецитабина (2500 мг/м2) в монорежиме для лечения больных с HR+HER2- мРМЖ, ранее получавших препараты таксанового ряда (исследование выполнено совместно с НМИЦ онкологии им. Н.Н. Петрова) [7].
Тезетаксел – новый препарат для приема внутрь таксаного ряда, назначаемый в дозировке 27 мг/м2 1 раз в 3 недели. В отличие от других препаратов таксанов, тезетаксел обладает более длительным периодом полувыведения и не нуждается в премедикации.
Ранее сообщались обнадеживающие результаты II фазы исследования по применению тезетаксела в монорежиме, ЧОО составила 45% и медиана ВБП – 5,4 мес. (Seidman et al, 2018 ASCO Annual Meeting).
В исследование были включены 685 больных ER+HER2- мРМЖ. Медиана ВБП составила 9,8 мес. в группе тезетаксел + капецитабин vs 6.9 мес. капецитабин в монорежиме (ОР 0,716; 95% ДИ 0,573-0,895; p=0,003). Частота объективных ответов составила 57% vs 41% (p=0,0002). Данные по ОВ ожидаются. Нейтропения была наиболее частым нежелательным явлением ≥3 степени (71,2% vs 8,3%). Отмена терапии в связи с нейтропенией или фебрильной нейтропенией в группе тезетаксел + капецитабин – 4,2%, в группе капецитабина – 1,5%. Частота развития нейропатии ≥3 степени – 5,9% vs 0,9%, алопеции ≥2 степени – 8,0% vs 0,3%. Следовательно, увеличение ВБП, а также удобство дозировки перорального препарата, отсутствие необходимости госпитализации, сравнительно низкая частота развития нейропатии ≥3 степени могут свидетельствовать в пользу применения тезетаксела в комбинации с редуцированной дозой капецитабина для лечения больных HR+HER2- мРМЖ.
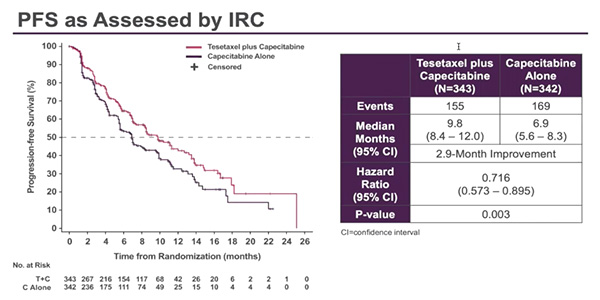
Рисунок 6. Исследование III фазы CONTESSA: Эффективность тезетаксела в комбинации
с редуцированной дозой капецитабина (1650 мг/м2) vs стандартная доза капецитабина (2500 мг/м2)
в монорежиме для лечения больных HR+HER2- метастатическим РМЖ, ранее получавших таксаны.
Определение циркулирующих опухолевых клеток при метастатическом РМЖ
Janni W. и соавт. доложены результаты метаанализа по изучению определения циркулирующих опухолевых клеток (ЦОК) с целью оценки ответа на лечение при метастатическом РМЖ [8]. В анализ были включены сведения о 3877 случаях с результатами оценки циркулирующих опухолевых клеток до начала лечения и спустя 29 дней после начала лечения. У 772 больных не определялись ЦОК как до, так и после начала терапии (neg/neg), у 286 больных наблюдалось приобретение ЦОК после лечения (neg/pos), у 1054 пациентов была отмечена конверсия из ЦОК+ в ЦОК- (pos/neg) и 1765 больных имели хотя бы одну ЦОК до и после начала терапии (pos/pos).
Медиана ОВ для групп neg/neg, neg/pos, pos/neg и pos/pos была 47,05, 29,67, 32,20, и 17,87 мес. (p<0,0001 для всех групп сравнения) соответственно. Отношения рисков (ОР) (референсная группа neg/neg) составили 1,74 (95% ДИ 1,43-2,10)для pos/neg группы, для neg/pos группы – 1,52 (95% ДИ 1,32-1,74) и для pos/pos группы – 3,15 (95% ДИ 2,78-3,57).
Таким образом, данные, полученные в ходе исследования, доказывают потенциальную возможность оценки ЦОК для оценки ответа на проводимую терапию для прогноза ОВ. Пациенты, у которых наблюдалось исчезновение ЦОК (pos/neg), имели значимое увеличение ОВ по сравнению с пациентами, у которых определялись ЦОК (pos/pos) как до, так и после лечения (32,20 vs 17,87 мес.). Однако некоторые эксперты признают, что данный метод пока не следует внедрять в клиническую практику, так как ранняя эскалация системного лечения с учетом результатов по ЦОК может вызвать неоправданное преждевременное исчерпание линий лекарственной терапии и увеличение токсичности от лечения. В перспективе определение циркулирующей опухолевой ДНК может позволить выбирать терапию в зависимости от наличия драйверных мутаций и тем самым значимо улучшить отдаленные результаты лечения.

Рисунок 7. Общая выживаемость в зависимости от статуса ЦОК
до начала лечения и после лечения.
ЗАКЛЮЧЕНИЕ
Прошедший с 8 по 11 декабря 2020 года симпозиум SABCS 2020 и Большая конференция RUSSCO «Рак молочной железы» 28-30 января 2021 года (в онлайн-формате) в очередной раз доказали, что системная терапия больных РМЖ сегодня – это комбинированная терапия с учетом биологического подтипа опухоли и таких важных мишеней, как рецепторы эстрогенов, экспрессия HER2, PD-L1-экспрессия, мутация PIK3CA и мутация gBRCA1/2, основанная на пациент-центрированном, проблемно-ориентированном, максимально индивидуализированном подходе.
Источники: