18.06.2018

В пленарную сессию конгресса ASCO 2018, на которой обычно представляются результаты самых значимых исследований в онкологии, были отобраны 4 работы. Одной из них оказался абстракт с долгожданными результатами рандомизированного исследования 3 фазы CARMENA. Задачей данного исследования было определить, нужна ли циторедуктивная нефрэктомия до назначения таргетной терапии больным метастатическим светлоклеточным почечно-клеточным раком (мПКР).
На протяжении последних 20 лет считалось, что удаление первичной опухоли вместе с почкой у пациентов без нефрэктомии в анамнезе значимо улучшает результаты последующего лекарственного лечения. Этот незыблемый стандарт был принят в эпоху цитокинотерапии с момента публикации результатов двух исследований, подтверждающих необходимость циторедуктивной нефрэктомии до назначения интерферона [1, 2]. По накатанной дороге в большинстве исследований эффективности таргетных препаратов нефрэктомия в анамнезе или циторедуктивная нефрэктомия были критериями включения. Крупные мета-анализы и ретроспективные исследования с участием тысяч пациентов в один голос утверждали, что удаление первичной опухоли до назначения таргетных препаратов представляется жизненно необходимым. Сомнения, высказываемые некоторыми группами и в единичных исследованиях [3-5], в частности о нецелесообразности нефрэктомии у больных с плохим прогнозом, игнорировались, и рекомендации, например, NCCN [6], оставались без изменений. И вот случилось исследование CARMENA [7], которое расставило все точки над i.
Пациенты с промежуточным и плохим прогнозом согласно критериям MSKCC были рандомизированы в группу циторедуктивной нефрэктомии с последующим назначением сунитиниба (N=226) или в группу только сунитиниба (N=224) без удаления первичной опухоли. По дизайну исследование носило характер noninferiority, то есть его целью было доказать отсутствие различий в эффективности двух подходов. Соотношение рисков смерти (HR) между группами не должно было превысить 1,2, и только в этом случае можно было бы сделать вывод о равной эффективности.
Медианы размера первичной опухоли и общей опухолевой массы, включая метастазы, составили 8,8/8,6 см и 14/14,4 см в группах нефрэктомия+сунитиниб / только сунитиниб соответственно. Чаще всего метастазы локализовались в легких (>70%), лимфатических узлах (35-39%) и костях (36-37%). У 6,7% больных, попавших при рандомизации в группу комбинированного лечения, так и не удалось выполнить циторедуктивную нефрэктомию, 17,7% больных не смогли получить сунитиниб. Во второй группе 4,9% больных не получили сунитиниб и 17% была выполнена нефрэктомия. В случае прогрессирования болезни в обеих группах последующее лечение проводилось у половины пациентов и было похожим (эверолимус или акситиниб).
При медиане наблюдения 50,9 мес. соотношение рисков смерти (HR) между группами составило 0,89, а следовательно, HR не превысил установленный показатель в 1,2, что свидетельствует о равной продолжительности жизни больных как при выполнении циторедуктивной нефрэктомии, так и без нее. Медиана общей выживаемости оказалась даже лучше у пациентов, получавших только сунитиниб, – 18,4 мес. против 13,9 мес. в группе нефрэктомии с последующим назначением сунитиниба (рис. 1). Тенденция сохранялась как в группе промежуточного прогноза (23,4 мес. против 19 мес.; HR=0,92), так и в группе плохого прогноза (13,3 мес. и 10,2 мес.; HR=0,86).
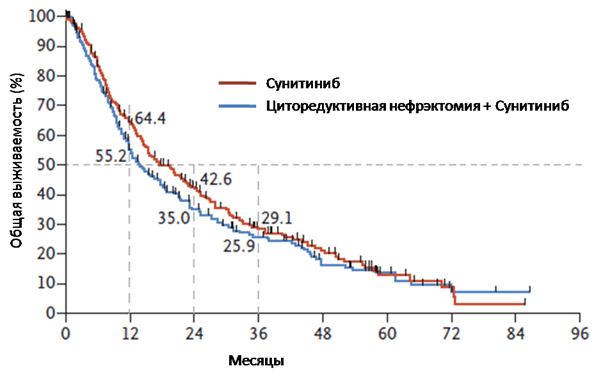
Рисунок 1. Общая выживаемость [7].
Медиана выживаемости без прогрессирования составила 8,3 мес. в группе только сунитиниба и 7,2 мес. в группе с нефрэктомией (HR=0,82). Частота объективных ответов была приблизительно одинаковой – 29,1% и 27,4% соответственно. Контроль над болезнью (сумма полных, частичных ответов и стабилизации) в течение 12 недель и более оказался достоверно лучше в группе без хирургического лечения – 47,9% по сравнению с 36,6% (P=0,02). Более того, пациенты с неудаленной первичной опухолью дольше получали сунитиниб (8,5 мес.), чем больные после нефрэктомии (6,7 мес.) (P=0,04). Частота нежелательных явлений 3-4 степени оказалась выше в группе только сунитиниба и составила 42,7%; 32,8% больных имели токсичность 3-4 степени в группе нефрэктомия+сунитиниб (P=0,04).
Несомненно, исследование CARMENA можно считать позитивным: первичная конечная точка – отсутствие различий в продолжительности жизни – была выполнена. Следовательно, циторедуктивная нефрэктомия до назначения сунитиниба представляется нецелесообразной у больных метастатическим светлоклеточным почечно-клеточным раком, имеющих промежуточный или плохой прогноз. Из исследования видно, что лекарственное лечение у пациентов с метастазами нужно начинать как можно скорее, потеря времени может приводить к худшим результатам контроля над болезнью, делает терапию сунитинибом менее продолжительной.
В самое ближайшее время мы можем ожидать изменений в практических рекомендациях. Из бурного обсуждения исследования в кулуарах становится понятно, что некоторые онкоурологи не будут готовы в одночасье отказаться от принятой ранее тактики и продолжат выполнять нефрэктомию до назначения лекарственного лечения. И они, возможно, окажутся правы в некоторых случаях.
Например, у больных с макрогематурией, болью, неконтролируемой гипертензией, паранеопластическим синдромом нефрэктомия сохранит свое значение. В этих случаях речь пойдет о паллиативной нефрэктомии. В России традиционно под термином «паллиативная нефрэктомия» подразумевалась как циторедуктивная нефрэктомия (чаще всего), так и непосредственно паллиативная нефрэктомия, направленная на уменьшение симптомов болезни. Возможно, в практике теперь эти два термина будут более четко разделены.
Остается неясным, нужно ли проводить хирургическое лечение больным с благоприятным прогнозом. Д-р Daniel George из Duke University, комментировавший данное исследование на ASCO, предположил, что результаты CARMENA можно экстраполировать на всю популяцию пациентов. Тем не менее, если строго следовать принципам доказательной медицины, то эффект отсутствия циторедукции в группе благоприятного прогноза доказан не был.
Как же быть с больными несветлоклеточным раком почки, у которых сунитиниб – тоже препарат выбора первой линии для промежуточного прогноза? Несколько месяцев назад на GU ASCO были представлены данные крупного ретроспективного анализа IMDC [8], в котором было показано, что циторедуктивная нефрэктомия у пациентов с метастатическим папиллярным раком почки увеличивает в 2 раза общую выживаемость – с 8,6 мес. до 16,3 мес. (HR=0,62; P<0,0001), с оговоркой о худших результатах в группе плохого прогноза.
Интересным представляется вопрос о необходимости нефрэктомии перед назначением других препаратов: темсиролимуса (стандарт терапии первой линии в группе плохого прогноза как светлоклеточного, так и несветлоклеточного рака почки [9]), комбинации ниволумаба и импилимумаба (недавно одобренной в США в качестве первой линии терапии больных с промежуточным и плохим прогнозом [10]), кабозантиниба (опция первой линии терапии пациентов с промежуточным и плохим прогнозом на основе результатов исследования CABOSUN [11]).
Да и вообще, как в практике отразятся результаты исследования на выборе препаратов первой линии? Будет ли чаще назначаться сунитиниб, показавший лучший результат у пациентов с плохим прогнозом, чем темсиролимус? А если на прием придет больной с неудаленной первичной опухолью и промежуточным/неблагоприятным прогнозом, что выберет врач – сразу назначит сунитиниб или отправит пациента на месяц на циторедуктивную операцию и через месяц начнет терапию ингибиторами контрольных точек? Или такой вариант – пациент после первой линии терапии сунитинибом остался с первичной опухолью, должны ли мы рассматривать циторедуктивную нефрэктомию перед второй линией терапии ниволумабом, акситинибом или ленватинибом в комбинации с эверолимусом? Все эти препараты изучались только у больных с предшествующей нефрэктомией [12-14].
Мы неожиданно столкнулись с изменением стандарта лечения метастатического рака почки, поэтому появилось много вопросов. Однако после представления результатов исследования CARMENA нет сомнений, что не требуется выполнение циторедуктивной нефрэктомии у пациентов с метастатическим светлоклеточным раком почки и промежуточным/плохим прогнозом. Циторедуктивная нефрэктомия не улучшает ни продолжительность жизни больных, ни выживаемость без прогрессирования, ни ответ на последующее лекарственное лечение и, более того, сопряжена с возможными хирургическими осложнениями и дополнительной нагрузкой на бюджет.
Литература: