19.09.2012
Н.В. Жуков
ФГБУ Федеральный научно-клинический центр детской гематологии,
онкологии и иммунологии им. Д. Рогачева МЗ и СР РФ;
ГБОУ ВПО Российский национальный исследовательский медицинский университет им. Н.И. Пирогова
Несмотря на то, что эндокринотерапия рака молочной железы (РМЖ) появилась задолго до возникновения такого модного сейчас понятия «таргетная терапия», она отвечает всем требованиям, позволяющим ей называться таргетной (целевой):
По признанию многих ведущих зарубежных онкологов, тамоксифен, одобренный для клинического применения еще в 1977 году, до настоящего времени остается образцом таргетного препарата.
В развитых странах мира именно эндокринотерапия является предпочтительным методом начального лечения подавляющего большинства больных, страдающих распространенным РЭ+РМЖ без висцерального криза. И это неудивительно, т.к. эндокринотерапия практически идеально подходит под задачи лечения этого заболевания, обеспечивая возможность значимого продления жизни больных без нанесения существенного урона ее качеству за счет токсичности самого лечения. При этом основным постулатом, присутствующим во всех международных рекомендациях, является то, что эндокринотерапия распространенного РЭ+РМЖ должна проводиться по возможности долго. При прогрессировании болезни на одном из эндокринных препаратов он должен меняться на альтернативный до того момента, пока доступный арсенал препаратов для эндокринотерапии не будет исчерпан. И подобный арсенал в настоящее время достаточно велик: антиэстрогены (SERM и SERD), ингибиторы ароматазы (стероидные и нестероидные), препараты для выключения функции яичников, прогестины и андрогены.
Даже после прогрессирования на фоне предшествующих линий эндокринотерапии определенная когорта больных продолжает отвечать на последующее лечение альтернативным препаратом и в ряде случаев – весьма длительной ремиссией. Это позволяет отнести РЭ+РМЖ к категории опухолей, которые, по меткому выражению предыдущего президента ASCO, являются глупыми, т.е. зависимы от одного пути стимуляции, блокада которого позволят добиваться значимых клинических успехов и длительно контролировать заболевание (см. рис. 1).

Рисунок 1. Умные и глупые опухоли
Однако очевидным является тот факт, что с каждой последующей сменой препаратов, воздействующих на один и тот же эстроген-зависимый путь стимуляции опухолевой клетки, доля больных, отвечающих на лечение, и медиана выживаемости без прогрессирования уменьшается. Это связано с тем, что опухоль «умнеет», т.е. вырабатывает резистентность к эндокринотерапии, которую уже не удается преодолеть путем простой замены эндокринопрепаратов. В такой ситуации единственным вариантом лечения до недавнего времени являлся переход на химиотерапию, позволяющую контролировать опухоль путем воздействия на «универсальные мишени» цитостатиков – геном и аппарат делений клетки.
К сожалению предпринимавшиеся до настоящего времени попытки отсрочить наступление резистентности к эндокринотерапии и/или преодолеть ее были малоуспешными. Попытки комбинации эндокринопрепаратов между собой или с химиотерапией, увеличение дозы эндокринопрепаратов, использование блокаторов дополнительных путей стимуляции опухоли либо не приносили успеха, либо его размер был слишком мал.
Весьма обнадеживающие данные о возможном выигрыше от комбинации двух эндокринопрепаратов с разным механизмом действия (фулвестрант и анастрозол) по сравнению с монотерапией анастрозолом были опубликованы по результатам исследования SWOG S0226 в 2011 году, а затем уточнены в 2012 [1]. В этом исследовании, включившем 707 больных, комбинация двух эндокринных препаратов привела не только к увеличению выживаемости без прогрессирования (с 13,5 до 15 мес., р=0,007), но и к тренду в отношении общей выживаемости (47,7 против 41,3 мес., р=0,05). Однако опубликованные следом результаты другого исследования FACT (n=514), имевшего весьма схожий дизайн и также сравнивавшего терапию анастрозолом с или без добавления фулвестранта, не выявили различий не только в общей выживаемости, но и в выживаемости без прогрессирования [2]. Выживаемость без прогрессирования в группе комбинированного лечения составила 10,8 мес., в группе сравнения 10,2 мес. (р=0,91). Общая выживаемость составила 37,8 и 38,2 мес. соответственно (р=1,0). Причины расхождения результатов этих двух весьма схожих исследований остаются не до конца понятными, но факт остается фактом – попытка улучшить результаты эндокринотерапии путем комбинации различных препаратов, воздействующих на один и тот же РЭ-опосредованный путь передачи стимулирующих сигналов, к сожалению, вновь не привела к достижению однозначного успеха.
Пожалуй, единственными относительно недавними успехами в попытках преодолеть резистентность, приведшими к регистрации препаратов, можно считать увеличение дозы фулвестранта с 250 мг до 500 мг на введение [3] и добавление анти-HER2 препаратов (лапатиниб и трастузумаб) к эндокринотерапии при коэкспрессии на опухолевых клетках РЭ и HER2 [4, 5]. Однако магнитуду выигрыша от этих манипуляций трудно назвать революционным достижением (рис. 2).
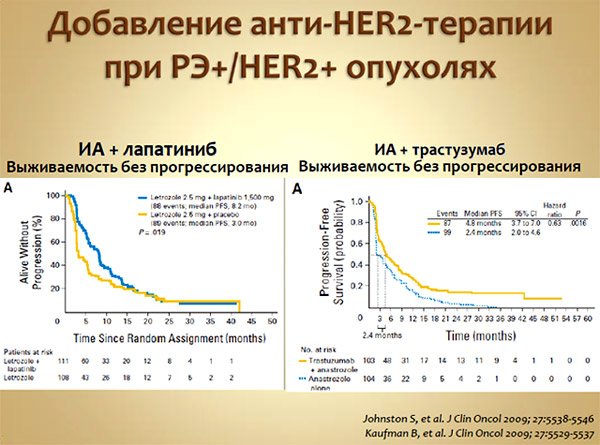
Рисунок 2. Добавление анти-HER2 терапии при РЭ+/HER2+ опухолях
И хотя нам было «приятнее» считать, что РЭ+РМЖ, характеризующийся относительно индолентным и длительным течением, является категорией болезни с «малыми» успехами от новых видов терапии, очевидным становилось, что в данном направлении отмечается явная стагнация.
На этом фоне очень неожиданными оказались результаты исследования TAMRAD, впервые опубликованные в 2010 г. В этом исследовании II фазы, включившем 111 больных распространенным РЭ+РМЖ, имевших прогрессирование болезни на фоне терапии ингибиторами ароматазы (в лечебном или адъювантном режиме), сравнивалась эффективность тамоксифена и комбинации тамоксифена с эверолимусом (препаратом из группы mTOR ингибиторов). Наш интерес к данному исследованию был обусловлен не столько тем, что в группе комбинированной терапии было показано увеличение частоты контроля над болезнью (61,1% против 42,1% в группе монотерапии тамоксифеном) и удвоение выживаемости без прогрессирования (8,5 vs 4,5 месяца) [6]. Различия в частоте контроля над болезнью и/или выживаемости без прогрессирования (хотя преимущественно и меньшей магнитуды) достаточно часто встречаются в исследованиях II фазы при РМЖ. Совершенно неожиданным оказался выраженный тренд в сторону улучшения общей выживаемости группы, получавшей комбинированную терапию (рис. 3). Эти результаты совсем не соответствовали сложившемуся отношению к распространенному РЭ+РМЖ как к индолентному, медленно текущему заболеванию с малыми успехами от новых видов терапии.
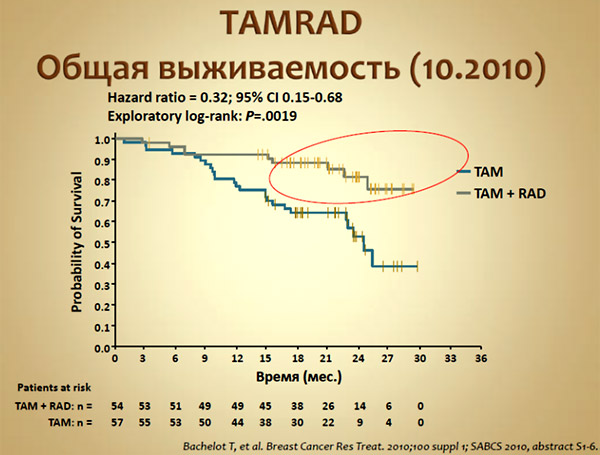
Рисунок 3. Результаты исследования TAMRAD
При этом различие в общей выживаемости при увеличении времени наблюдения за больными не только не уменьшилось, но и достигло уровня статистической значимости (р=0,007) при последующем запланированном анализе, данные которого были опубликованы в 2012 году [7].
Результаты исследования TAMRAD были интересны нам и в связи с тем, что согласно предклиническим исследованиям использование mTOR ингибиторов позволяло надеяться на достижение торможения сразу нескольких сигнальных путей, не принадлежащих к РЭ-зависимой оси стимуляции и, соответственно, отвечающих за развитие истинной резистентности, которую нельзя преодолеть простой сменой эндкоринопрепаратов. Одновременно, mTOR оказался активным игроком и в пределах РЭ+ зависимого пути, отвечая за «внутреннюю резистентность» к эндокринотерапии: mTOR комплекс-1 (mTORC1) за счет активации киназы S6 приводит к фосфориляции одного из внутриклеточных доменов рецептора эстрогена, что в свою очередь ведет к его лиганд-независимой активации (автономной активности).
Результаты этих исследований послужили основой для проведения рандомизированного, двойного слепого исследования III фазы – BOLERO-2.
В исследование было включено 724 постменопаузальных (в естественной или индуцированной менопаузе) пациентки с РЭ+, HER2-негативным распространенным РМЖ. Для включения в исследования необходимо было наличие заболевания, расцениваемого как резистентное к терапии нестероидными ингибиторами ароматазы (летрозол или анастрозол). В данном исследовании резистентными считались больные, у которых прогрессирование болезни отмечалось:
Допускалось наличие в анамнезе терапии другими эндокринопрепаратами (антиэстрогены получили около 60% больных, включенных в исследование) и одного режима лечебной химиотерапии. Висцеральные метастазы имелись у 56% больных, более трети пациенток имели ≥3 областей метастатического поражения.
Больные, отвечающие критериям отбора, рандомизировались на получение стероидного ингибитора ароматазы (экземестан 25 мг/сут) в комбинации с плацебо или эверолисусом в дозе 10 мг/сут (в соотношении 2:1 в пользу комбинации эверолимус + экземестан). Первичной целью исследования являлась выживаемость без прогрессирования, вторичными целями – общая выживаемость, частота достижения объективного ответа и контроля над болезнью. Помимо выживаемости и эффективности в исследовании оценивалось время до ухудшения общего состояния больных, переносимость лечения и качество жизни.
Частота достижения объективного ответа (полная + частичная регрессия) были невелики в обеих группах: 7,0% в группе комбинированной терапии против 0,4% в контрольной группе, однако различалась статистически значимо (р<0,001). Однако гораздо более важным с нашей точки зрения явилась способность эверолимуса преодолевать развитие «ранней» резистентности, т.е. ситуации, когда наилучшим ответом на лечение является прогрессирование болезни. По результатам независимой центральной оценки в группе, получавшей экземестан с плацебо, каждая пятая пациентка (21,8%) вообще не ответила на лечение, в то время как в группе, получавшей дополнительно к эземестану эверолимус, таких больных было лишь 5,6%. Длительность «удержания ответа» на лечение также была значимо выше в группе комбинированного лечения. При оценке исследователями на момент проведения в феврале 2011 г. запланированного анализа [8] медиана времени до прогрессирования у больных, получавших комбинированную терапию, составила 6,9 месяцев против 2,8 месяцев в группе, получавшей экземестан + плацебо (HR 0,43, p<0,001). По оценке независимых экспертов это различие было еще более значимым: 10,6 месяцев и 4,1 месяцев соответственно (HR 0,36, p<0,001). При дальнейшем наблюдении за больными, как и в исследовании TAMRAD, отмечается тенденция к еще большему расхождению кривых выживаемости. Как хорошо видно из рисунка 4, при оценке независимыми исследователями более чем у 45% больных в группе комбинированной терапии контроль над болезнью сохраняется и спустя год после начала лечения.
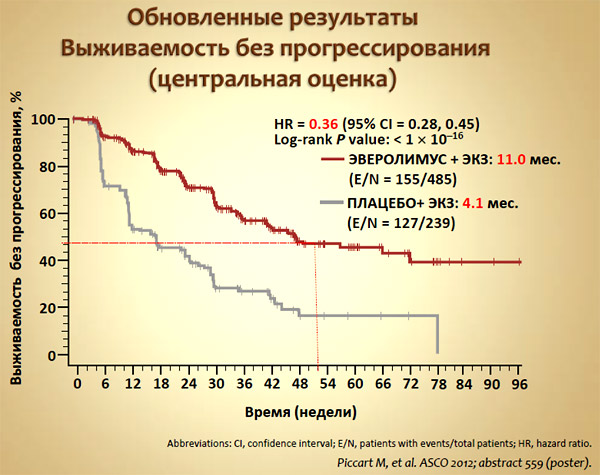
Рисунок 4. Результаты исследования BOLERO-2.
Оценить общую выживаемость пока не представляется возможным ввиду малого числа отрицательных событий (10,7% в группе комбинированной терапии против 13% в группе сравнения) на данных сроках наблюдения.
Разумеется, следует отметить, что прибавка в выживаемости без прогрессирования у больных, получавших эверолимус + экземестан, была сопряжена и с большей частотой нежелательных явлений. У больных, получавших эверолимус, чаще встречались такие осложнения, как стоматиты, анемия, гипергликемия, неинфекционные пневмониты различной степени тяжести. И хотя каких-либо новых, не характерных для mTOR-ингибиторов нежелательных явлений в данном исследовании выявлено не было, развитие побочных эффектов в группе эверолимуса значимо чаще приводило к необходимости редукции дозы или даже к необходимости досрочного прекращения терапии (4% в группе экземестана против 19% в группе комбинированной терапии). Чаще среди больных, получавших комбинированное лечение, отмечался и досрочный отзыв информированного согласия (5% против 2% в группе сравнения). Таким образом, почти четверть пациенток, включенных в исследование, прекратили терапию эверолимусом до наступления прогрессирования заболевания. Но, как наглядно видно на рисунке 4, это не помешало препарату значительно изменить течение болезни у большинства больных и добиться длительного контроля заболевания. Более того, развитие дополнительных побочных эффектов при обеспечении адекватного наблюдения за больными и своевременной коррекции доз не привело к ухудшению качества жизни больных.
Результаты исследования BOLERO-2 позволили зарегистрировать эверолимус по показанию «Лечение пациенток в постменопаузе с гормонзависимым распространенным раком молочной железы в комбинации с ингибиторами ароматазы, после предшествующей эндокринной терапии» сначала в Российской Федерации, а затем и в США и ЕС.
Появление подобной терапевтической опции для лечения распространенного РЭ+РМЖ является отрадным событием само по себе. Однако еще более приятным является то, что в лечении распространенного РЭ+РМЖ, уже достаточно давно (практически – с момента создания тамоксифена) воспринимаемого как опухоль с малыми успехами от новых видов терапии, достигнуто действительно клинически значимое улучшение результатов лечения.
Литература