Новости онкологии Уголок радиотерапевта
11.09.2023
В самом конце августа в Красном журнале ASTRO (International Journal of Radiation Oncology, Biology & Physics) появилась статья, причем в открытом доступе, хоть и не в окончательном варианте, принятая к публикации буквально недавно с рекомендацией дополнить ряд данных, поэтому на страницах стоит штамп «Journal Pre-proof». Чем же так интересна эта работа?
Это исследование 2 фазы от голландских авторов с интригующим названием PAINPANC, посвященное противоболевой роли локальных методов, прежде всего лучевой терапии, при раке поджелудочной железы (РПЖ). Не стоит говорить об известном коварстве этой опухоли и ее крайней неподатливости существующим методам лечения. Мы также прекрасно знаем о разнообразии негативной симптоматики местнораспространенного и метастатического рака поджелудочной железы, с которой сложно бороться. Большинство (70-80%) пациентов жалуются на боль из-за опухолевой инфильтрации чревного сплетения, обструкции или растяжения протоков и воспаления в окружающих тканях; эта крайне неприятная боль обычно локализуется в эпигастральной области и/или иррадиирует в спину. Интенсивность боли зачастую варьирует от умеренной до сильной, и ее довольно сложно регулировать. В целом, наряду с другими симптомами запущенного заболевания, это приводит к крайне плохому общему качеству жизни (QoL).
Несколько лечебных подходов были призваны бороться с подобной болью: применение обезболивающих фармакологических препаратов, химиотерапия и/или лучевая терапия и блокада чревного сплетения. Опиаты применяются как правило для купирования умеренной и тяжелой рефрактерной боли, однако использование сильных опиатов часто вызывает побочные эффекты, которые могут привести к тяжелым последствиям и дальнейшему снижению качества жизни. Лучевая терапия способна уменьшить боль, связанную с опухолью, и даже снизить дозу наркотических анальгетиков, однако роль метода явно недооценена на протяжении десятилетий.
По данным крупного ретроспективного анализа канадских авторов [1], основанного на результатах лечения 2623 больных раком поджелудочной железы, из которых у большинства (62%) был отмечен сильный болевой синдром, основная роль в купировании боли принадлежит именно опиатам (75,6% таких пациентов получали только обезболивающие препараты), тогда как значение локальных методов (ЛТ и нервная блокада) остается недооцененным (лишь 13,5% получали ЛТ и 1,2% – хирургическую блокаду). Авторы продемонстрировали, что значимое уменьшение болевого синдрома было отмечено у 62% больных, получавших только опиаты, у 73% получивших противоболевую ЛТ и у всех пациентов после хирургической нервной блокады, при этом удачное купирование болевого синдрома даже позитивно отразилось на результатах выживаемости (рис.1).
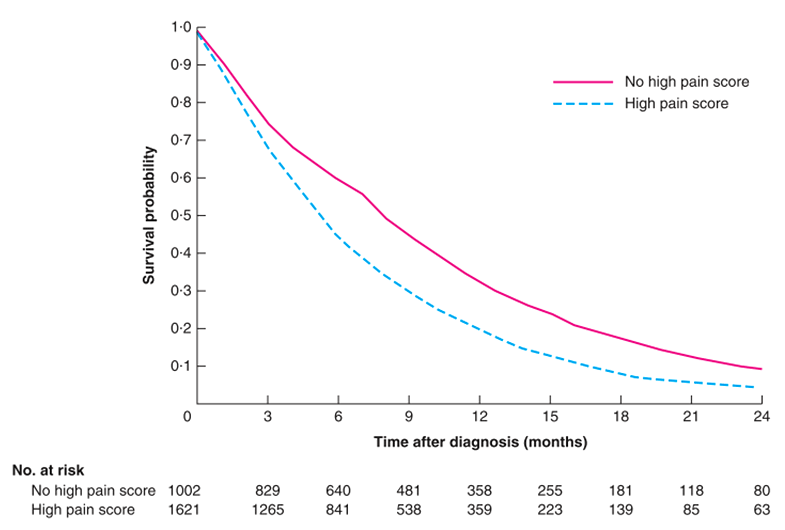
Рисунок 1. Показатели выживаемости некурабельных больных РПЖ в зависимости от выраженности (и степени купирования) болевого синдрома (p<0,001) [1].
На рисунке 2 представлена шкала изменений болевого синдрома в зависимости от выбранного метода его купирования – применения наркотических анальгетиков или ЛТ.
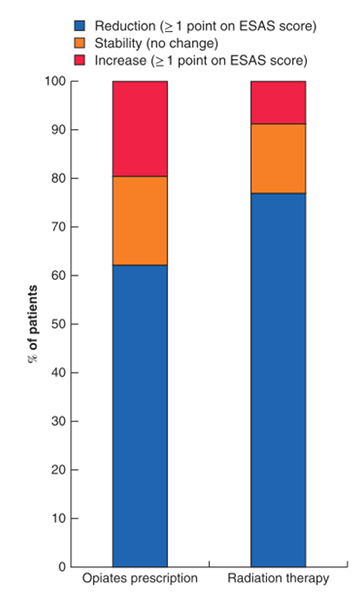
Рисунок 2. Динамика болевого синдрома после применения опиатов и ЛТ.
Без сомнения, эти данные должны привлечь внимание к выбору альтернативных методов эффективного купирования болевого синдрома у этой сложной категории больных, нежели простого назначения сильных обезболивающих препаратов со всеми вытекающими из этого последствиями. Поэтому голландские авторы сконцентрировались на оценке эффективности паллиативного короткого курса ЛТ у некурабельных пациентов с местнораспространенным и распространенным РПЖ с болевым синдромом.
Ряд более ранних ретроспективных и проспективных наблюдательных исследований продемонстрировали, что короткие курсы радиотерапии способны уменьшить болевой синдром при РПЖ, однако качественная оценка, на основании валидированных опросников, не проводилась. Целью этого проспективного нерандомизированного исследования II фазы было оценить изменение интенсивности боли (как первичный результат) и общее качество жизни (вторичная конечная точка), причем многократно, через определенные промежутки времени, во время короткого курса паллиативной лучевой терапии и последующего наблюдения, с использованием валидированных пациенто-ориентированных оценочных шкал у больных РПЖ с болевым синдромом, связанным с опухолью и рефрактерным к обезболивающим препаратам. Кроме того, острая токсичность и общая выживаемость также были оценены авторами.
В проспективном нерандомизированном исследовании 2 фазы PAINPANC 29 больных РПЖ с болевым синдромом получали короткий курс ЛТ (24 Гр за 3 фракции, 1 фракция в неделю) в период с 2015 по 2018 гг. Подавляющее большинство пациентов имели статус ECOG-ВОЗ ≥1 (n=27, 90%), 56,7% (n=17) имели отдаленные метастазы, а у 63,3% (n=19) опухоль располагалась в головке поджелудочной железы. Восемь пациентов (26,7%) не получили общую дозу ЛТ в 24 Гр из-за клинического ухудшения или прогрессирования опухоли. Болевой синдром у всех пациентов был рефрактерен к обезболивающим препаратам. Первичная конечная точка определялась как клинически значимое среднее снижение интенсивности боли на ≥2 балла по сравнению с исходным уровнем, в течение семи недель после начала лечения. Вторичной конечной точкой была оценка глобального качества жизни с клинически значимым увеличением на 5-10 баллов (по шкале 0-100). Уменьшение боли и изменение качества жизни оценивались девять раз с использованием Краткого опросника боли и опросника EORTC-QoL-C15-PAL.
Из всех пациентов, получавших лучевую терапию, снижение приема обезболивающих препаратов оказалось возможно у 16 больных (55,2%) во время лечения и дальнейшего наблюдения. У шести пациентов (20,7%) объем обезболивания оставался неизменным, а пяти пациентам (17,2%) потребовалось увеличение назначения опиоидных препаратов на ≥25%, из которых три пациента сообщили об уменьшении приема обезболивающих препаратов в течение периода наблюдения. Коррекция обезболивающих препаратов неизвестна у двух пациентов (6,9%), оба получали только одну фракцию лучевой терапии. Исходно средняя эквивалентная суточная доза перорального морфина составила 129,5 мг (диапазон 20,0-540,0 мг), после облучения она снизилась до 75,0 мг (диапазон 15,0-360,0 мг), P=0,021. Боль уменьшилась в среднем на 3,15 балла от исходного уровня к седьмой неделе (P=0,045). Пациенты сообщили о клинически значимом снижении средней интенсивности боли с 5,9 до 3,8 балла (P=0,011) в течение первых трех недель, которое далее снижалось до 3,2 до 11-й недели и в итоге заканчивалось на 3,4 балла (P=0,006) на 21-й неделе после первой фракции лучевой терапии. Глобальное качество жизни значимо улучшилось с 50,5 до 60,8 за период наблюдения, P=0,001 (рис.3). Острая токсичность 3 степени наблюдалась у трех пациентов (преимущественно слабость и тошнота/рвота), токсичности 4-5 степени не наблюдалось. Медиана ОВ составила 11,8 недель, а одногодичная выживаемость – 13,3%.
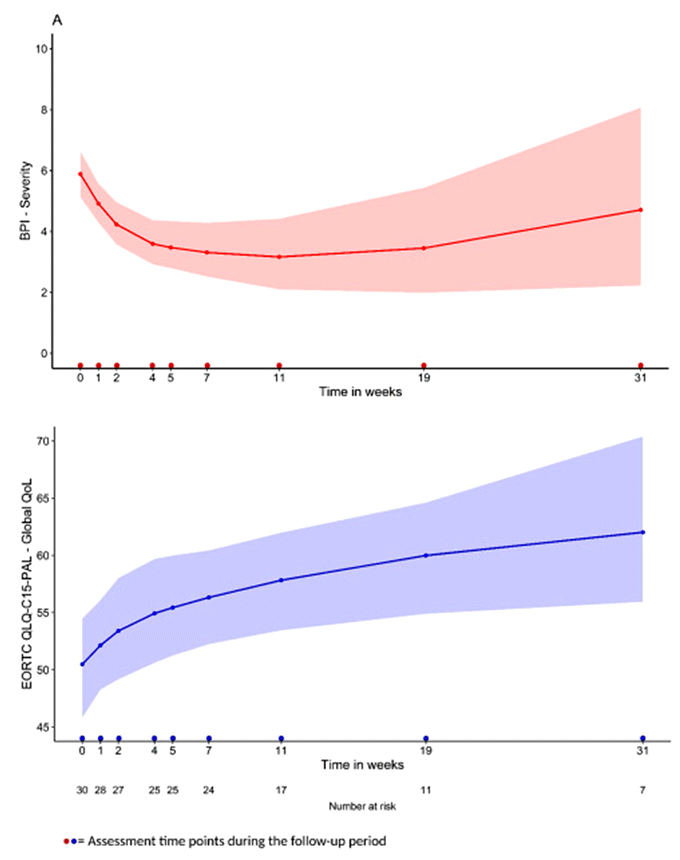
Рисунок 3. Прогнозируемые средние баллы по А) интенсивности боли и Б) общему качеству жизни с течением времени. Заштрихованная область представляет 95% доверительные интервалы. Временные точки оценки: исходно (0 = до начала лучевой терапии) и в течение периода наблюдения (до второй и третьей фракций лучевой терапии, через 4, 5, 7, 11, 19 и 31 неделю после первой лучевой терапии).
В заключение авторы сделали вывод, что, возможно, роль лучевой терапии при распространенном РПЖ незаслуженно недооценена, поскольку это пусть и небольшое проспективное нерандомизированное исследование II фазы продемонстрировало возможность быстрого и клинически значимого снижения интенсивности болевого синдрома у большинства пациентов после короткого курса ЛТ и повышение общего качества жизни, продолжающееся практически до финала жизни ценой преимущественно умеренной и преходящей острой токсичности. Положительный результат исследования и воспроизводимость лечения могут и должны быть использованы для возмещения расходов на паллиативное облучение для подобной группы больных. Для подтверждения этих данных, без сомнения, необходимо проведение более крупных исследований.
Источники: