04.06.2023
На конгрессе были представлены обновленные результаты исследования 3 фазы [1], посвященные изучению эффективности золбетуксимаба (IgG1 к CLDN18.2) в комбинации с химиотерапией в первой линии лечения HER2-негативного, CLDN18.2-позитивного диссеминированного рака желудка.
Первичной конечной точкой работы была выживаемость без прогрессирования (ВБП). В исследование было рандомизировано 2333 больных, экспрессия CLDN18.2 выявлена в 38,4% случаях (n=808). Всего в клиническое исследование было включено 507 больных.
При медиане времени наблюдения в 12 мес. добавление золбетуксимаба к химиотерапии СAPOX позволило статистически значимо увеличить медиану ВБП с 6,8 до 8,21 мес. (p=0,0007) (рис.1) и медиану ОВ с 12,16 до 14,39 мес. (p=0,0118).
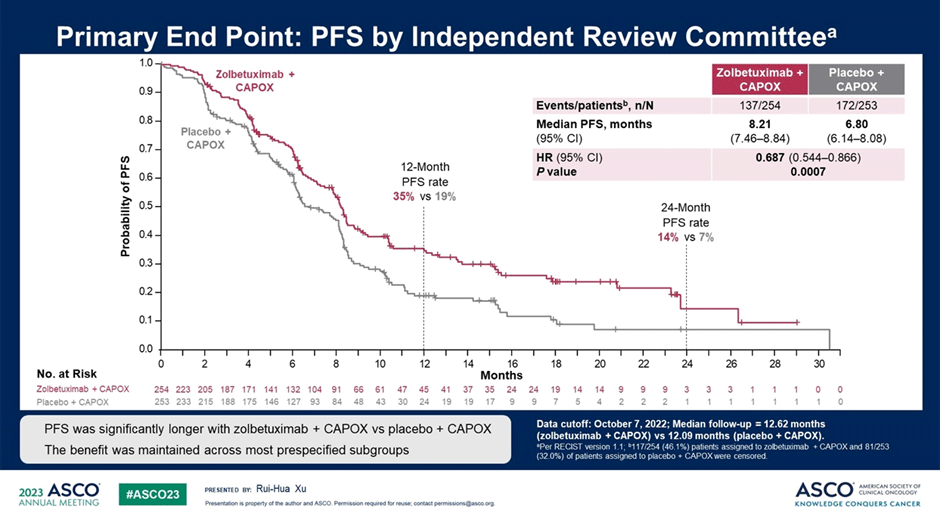
Рисунок 1. График выживаемости без прогрессирования.
Частота объективного ответа (ОО) в группе с золбетуксимабом достигла 53,8%, в группе только химиотерапии – 48,8%, при контроле роста опухоли (КРО) в 77,4% и 76,6% соответственно.
НЯ зарегистрированы у 98,8% больных в группе с золбетуксимабом и у 98,8% в группе только химиотерапии, а НЯ 3 степени и выше в 72,8% и в 69,9% случаях соответственно и были преимущественно представлены тошнотой (8,7% против 2,4%), рвотой (12,2% против 3,6%), анемией (10,6% против 11,2%), тромбоцитопенией (7,5% против 8,0%) и нейтропенией (7,1% против 2,8%). К сожалению, 6 больных в группе с золбетуксимабом и 7 пациентов в группе стандартной терапии погибли из-за НЯ, связанных с лечением.
На конгрессе также представлена небольшая работа о конъюгате антитела (IgG1) к рецептору CLDN18.2 и MMAE (монометил ауристатин E) [2]. В настоящий момент в исследование 1 фазы включено 33 пациента, ранее получавших стандартную терапию (78,8% – рак желудка). Частота ОО составила 38,1% при КРО в 57,1%. Опубликованы данные о токсичности лечения. НЯ были преимущественно представлены тошнотой (42,4%), рвотой (36,4%), сухостью глаз (21,2%) и анемией (21,2%).
Krystal-1 [3] – мультикогортное исследование, в которое были включены пациенты со злокачественными опухолями желудочно-кишечного тракта с мутацией в гене KRASG12C. Мутация в гене KRASG12C встречается при раке легкого (до 14%), аппендикса (3-4%), билиарного тракта (1%), аденокарциноме поджелудочной железы (1-4%), колоректальном раке (3-4%) и т.д. Адаграсиб – ингибитор KRASG12C, в настоящий момент одобрен FDA в терапии рака легкого с мутацией KRASG12C.
В работу включались пациенты с различными злокачественными новообразованиями с мутацией в гене KRASG12C, ранее получившие стандартные методы лечения. Больные получали адаграсиб 600 мг 1 раз в день до прогрессирования или неприемлемой токсичности. Первичной конечной точкой исследования была частота ОО.
У большинства пациентов, включенных в работу, была аденокарцинома поджелудочной железы (n=21), в 12 случаях первичный очаг локализовался в билиарном тракте и у 10 больных – в аппендиксе.
Частота ОО составила 35,1%, а медиана длительности ответа – 5,3 мес. При опухолях желудочно-кишечного тракта частота ОО оказалась равной 16,7% (рис. 2).
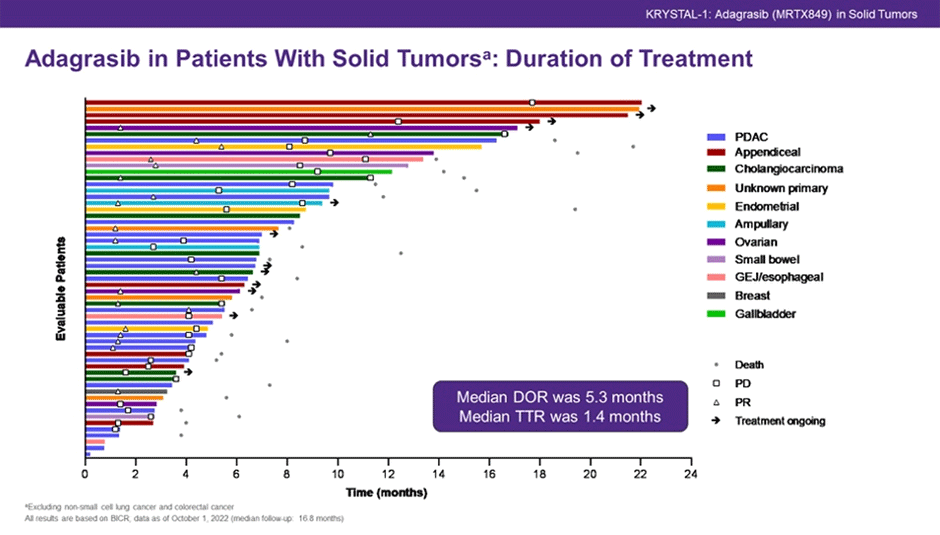
Рисунок 2. Результаты исследования Krystal-1.
При медиане времени наблюдения в 16,8 мес. медиана ВБП в общей группе достигла 7,4 мес., у больных РПЖ – 5,4 мес., при злокачественных новообразованиях билиарного тракта – 8,6 мес. Медиана ОВ в общей группе составила 14,0 мес., у больных РПЖ – 8,0 мес., при злокачественных новообразованиях билиарного тракта – 15,1 мес.
НЯ любой степени зарегистрированы у 96,8%, редко превышали 1-2 степени и были преимущественно представлены тошнотой (49,2%), диарей (47,6%), слабостью (41,3%), рвотой (39,7%), повышением уровней креатинина (15,9%) и АСТ (14,3%), анемией (14,3%).
Источники: