Новости онкологии «А вот был у меня случай…», или «Охотничьи записки» онкологов
10.05.2023




Олигопрогрессия представляет собой клиническую ситуацию, при которой отмечается прогрессирование ограниченного количества метастатических очагов (пять или менее).
В клинической практике стандартный подход при прогрессировании метастатического заболевания заключается в смене линии системной терапии, без различий между олигометастатическим и полиметастатическим прогрессированием. Однако последовательная смена линий системной терапии обычно связана с сокращением интервала времени до прогрессирования и нарастанием токсичности от системного лечения.
В последнее время применение стереотаксической аблативной лучевой терапии (SABR) все чаще рассматривается в контексте олигопрогрессии метастатического почечноклеточного рака (мПКР), как правило, с целью продления текущей системной терапии и экономии последующих линий системного лечения.
Schoenhals et al. [1] представили результаты лечения 36 пациентов со светлоклеточным мПКР с олигопрогрессией из группы с благоприятным риском (27,8%) или промежуточным риском (61,1%) IMDC. SABR была выполнена на олигопрогрессирующие очаги (от 1 до 3) вне зависимости от общего количества метастатических очагов, после чего пациенты продолжали получать текущую линию терапии до прогрессирования. При дальнейшем прогрессировании у 11 пациентов также были отмечены олигопрогрессирующие очаги, на которые проводились повторные сеансы SABR. Медиана модифицированной выживаемости без прогрессирования (мВБП) от момента SABR до прогрессии составила 9,2 мес., медиана общей выживаемости от момента SABR до прогрессии – 43,4 мес. В этом исследовании авторами также было продемонстрировано, что проведение SABR во время лечения ингибиторами контрольных точек (ИКТ) было связано с более длительной ВБП (>28,4 мес., p=0,0001) по сравнению с ингибиторами mTOR или ингибиторами VEGF. На основе этих многообещающих результатов та же команда исследователей из MDACC разработала исследование фазы II [2], в которое были включены 20 пациентов с мПКР, получавшие различные линии системной терапии (с первой по четвертую). У большинства пациентов были синхронные метастазы (60%), и всем этим пациентам была выполнена циторедуктивная нефрэктомия. При включении в исследование системная терапия была представлена ИКТ у 8 больных, ИТК также у 8 пациентов и комбинированными схемами лечения у 4 пациентов. Через 1 год 44,2% больных оставались на той же линии системной терапии. Медиана времени от SABR до начала новой линии системной терапии (мВБП) составила 11,1 мес., при этом медиана времени от начала системной терапии до прогрессирования и перехода на другую линию (SABR-aided systemic therapy) оказалась 24,4 мес. Выживаемость без прогрессирования на текущей линии лекарственной терапии составила 84,7% в течение 1 года и 50,8% – в течение 2 лет. Cheung et al. [3] сообщили о сходных результатах в проспективном исследовании у пациентов с олигопрогрессией на системной терапии ИТК. Тридцать семь больных с мПКР были включены в этом исследование и пролечены по поводу 57 олигопрогрессирующих очагов. У большинства (54%) были метахронные олигометастатические очаги и заболевание IMDC промежуточного риска (68%). Медиана продолжительности терапии ИТК до олигопрогрессии составила 18,6 мес., что больше показателей, полученных в исследовании Checkmate-214 [4] и Keynote-426 [5] (8,4 и 11,1 мес. соответственно). Медиана длительности сохранения текущей линии системной терапии составила более 1 года.
Пациенты с более индолентным развитием метастатического процесса [3], а также с меньшим общим количеством метастатических очагов на момент проведения SABR [2], вероятно, получают наибольший выигрыш в выживаемости по сравнению с другими пациентами с олигопрогрессией мПКР при проведении SABR на отдельные очаги.
Клинический случай
Пациент К, 1984 г.р., некурящий. Заболел с января 2011 года (на тот момент ему было лишь 27 лет), когда отметил примесь крови в моче. При обследовании выявлено объемное образование правой почки. В феврале 2011 г. выполнена радикальная нефрэктомия справа. Гистологическое исследование показало светлоклеточный гипернефроидный рак Grade 3, c врастанием опухоли в капсулы почки, но без инвазии в просвет лоханки, в 5 исследованных лимфоузлах без признаков опухолевых клеток. Стадия II – T2N0M0. С февраля 2011 по 2016 г. пациент находился только под динамическим наблюдением.
В августе 2016 г. отмечено прогрессирование заболевания. По данным КТ выявлены множественные метастатические очаги в легких, лимфоузлах средостения, печени, лимфоузлах ворот печени, по брюшине. Их общее количество превышало 100.
С августа 2016 г. начата таргетная терапия Сутентом (сунитиниб) в дозе 50 мг. По данным контрольных обследований в ноябре 2016 г. отмечена частичная регрессия очагов вплоть до полной регрессии части из них, без признаков дальнейшего прогрессирования, однако у пациента присутствовал ладонно-подошвенный синдром 2 степени, а также практически постоянный сухой, непродуктивный кашель, вероятнее всего, связанный с наличием увеличенного бифуркационного лимфоузла размером 2,7×1,6×2,8 см.
В рамках клинического исследования Ib фазы (VOLGA Study [6]) по изучению безопасности и эффективности стереотаксической лучевой терапии (SBRT) у пациентов с экстракраниальными метастазами почечноклеточного рака, получающих стандартную таргетную терапию или иммунотерапию ингибиторами контрольных точек, в ноябре 2016 г. в Ульяновском областном клиническом онкологическом диспансере пациенту была проведена стереотаксическая 3D-конформная лучевая терапия (SBRT) на область бифуркационного лимфоузла в средостении с РОД 6 Гр, 5 сеансов до СОД 30 Гр. За время лечения были отмечены только явления лучевого эзофагита 1 ст., которые успешно разрешились при консервативном лечении. После курса SBRT пациент продолжил прием сунитиниба до октября 2020 г., при этом кашель постепенно уменьшился, несмотря на то, что по размерам облученный лимфоузел оставался стабильным.
В ноябре 2020 г. отмечен первый эпизод олигопрогрессии в виде роста единичного метастатического очага во втором ребре справа, сопровождавшегося патологическим переломом. С декабря 2020 по март 2021 г. пациент получил 3 курса иммунотерапии по схеме ниволумаб + ипилимумаб с последующей стабилизацией опухолевого процесса. С апреля 2021 г. пациент продолжает получать ниволумаб по настоящее время в поддерживающем режиме.
В феврале 2022 г. отмечен второй эпизод олигопрогрессии в виде увеличения метастатического очага в S3 правого легкого, появления во 2 ребре справа остеолитического компонента, увеличения мягкотканного компонента метастатического очага в правой подвздошной кости (рис.1).
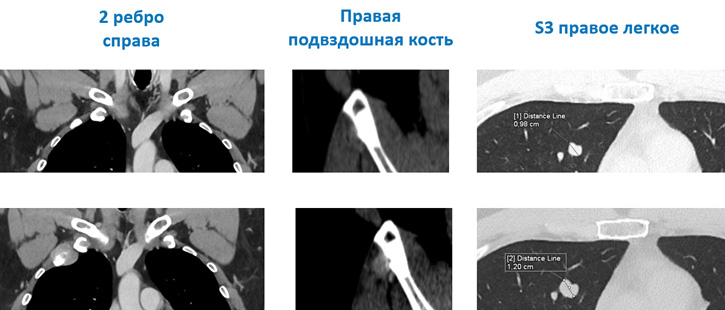
Рисунок 1. Олигопрогрессия на фоне поддерживающей терапии ниволумабом.
Учитывая олигометастатическое прогрессирование, на междисциплинарном консилиуме института онкологии Хадасса Москва пациенту был рекомендован курс стереотаксической аблативной лучевой терапии (SABR) на олигопрогрессирующие очаги и продолжение текущей линии лекарственной терапии (ниволумаб). В мае 2022 г. в клинике Хадасса Москва проведена SABR по протоколу однократного облучения высокой разовой дозой (Single-Dose Radiation Therapy) 24 Гр на очаг во 2 ребре справа и очаг в крыле правой подвдошной кости с мягкотканным компонентом, 28 Гр на очаг в S3 правого легкого (рис.2).
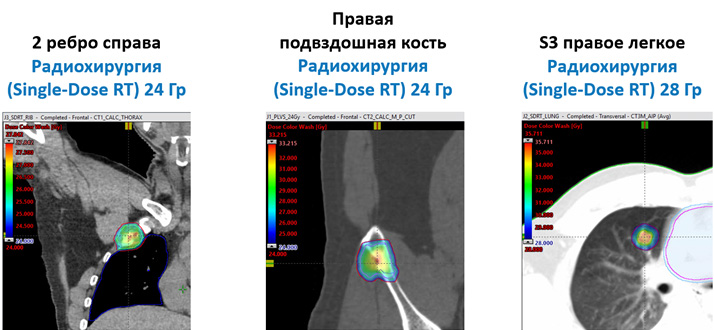
Рисунок 2. SABR на 3 очага олигопрогрессии (май 2022 г.).
Далее пациент продолжил получать ниволумаб. По данным контрольных обследований отмечена стабилизация заболевания: отсутствие новых очагов, постепенное уменьшение размеров облученных очагов (рис.3).
В марте 2023 г. отмечен третий эпизод олигопрогрессии в виде продолженного роста метастатического очага в заднем отрезке 2-го ребра справа, также выявлено увеличение параэзофагеального лимфоузла на уровне нижнегрудного отдела пищевода (рис.4). При этом отмечен полный рентгенологический ответ по ранее пролеченному очагу в S3 правого легкого (только признаки постлучевого фиброза легкого на месте очага), а также полный ответ мягкотканного компонента ранее облученного очага в крыле правой подвздошной кости.
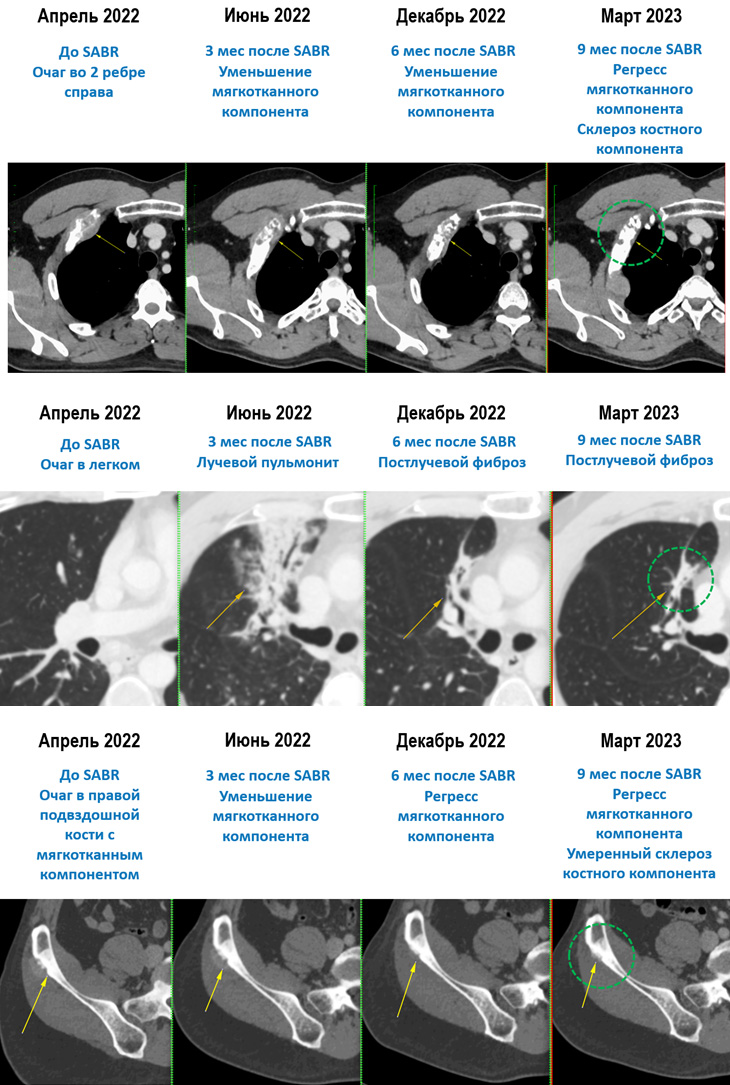
Рисунок 3. Динамика со стороны очагов, пролеченных в мае 2022 г.
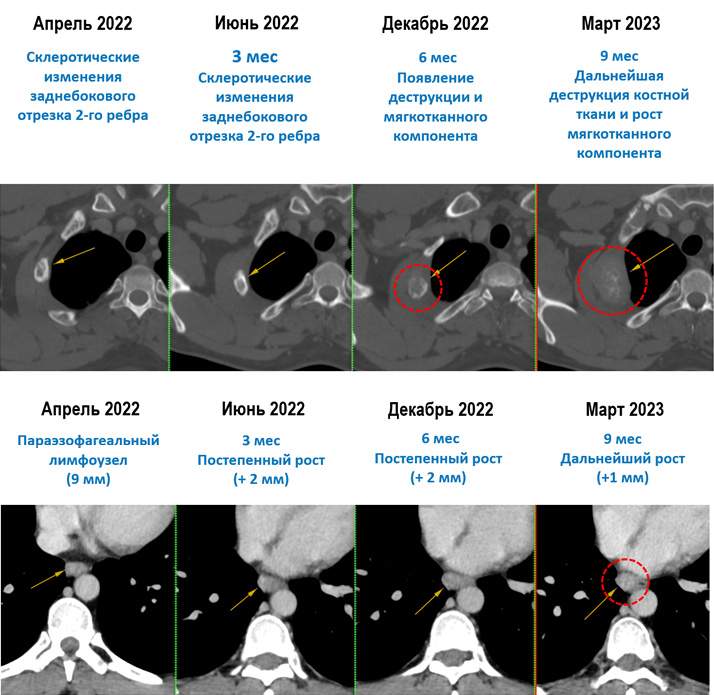
Рисунок 4. Олигопрогрессирующие очаги.
Учитывая повторное олигопрогрессирование на прежней линии лекарственной терапии, на консилиуме Института онкологии Хадасса было рекомендовано проведение повторного курса SABR на метастатический очаг в заднем отрезке 2-го ребра справа и метастатический очаг в параэзофагеальном лимфоузле на уровне нижне-грудного отдела пищевода до СОД 35 Гр, РОД 7 Гр, 5 сеансов, а также продолжение иммунотерапии ниволумабом.
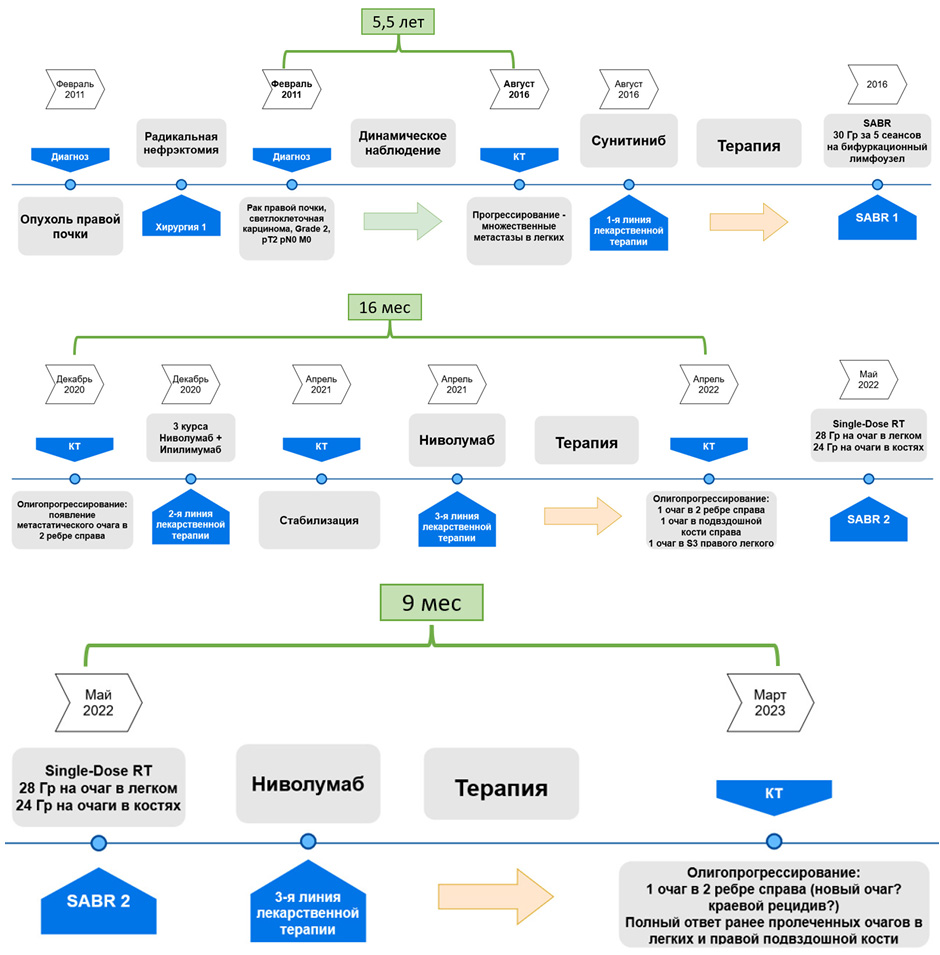
Рисунок 5. Пациент К.: течение заболевания и лечения, общая схема.
Таким образом, в данном случае у пациента с множественными метастатическими очагами почечноклеточного рака удалось продлить текущую, вторую линию лекарственной терапии ингибиторами контрольных точек (ниволумаб) как минимум на 9 мес. от момента стереотаксической аблативной лучевой терапии на 3 олигопрогрессирующих очага, а общая длительность текущей линии системной терапии на данный момент составила более 24 мес. У пациента отмечена хорошая переносимость лечения, отсутствие каких-либо серьезных нежелательных явлений как со стороны очагов, пролеченных с помощью лучевой терапии однократной высокой разовой дозой (Single-Dose RadioTherapy), так и хорошая переносимость лекарственного лечения в целом.
Этот клинический случай не доказывает сам по себе, что применение SBRT приведет к улучшению в общей выживаемости пациента, однако ее своевременное применение, дающее возможность продолжить ниволумаб и поддерживать локальный контроль заболевания, несомненно, придало сил и надежды пациенту и команде его онкологов, поскольку это отсрочило необходимость менять курс системного лечения. Такие клинические случаи генерируют гипотезу об эффекте аблативной ЛТ при олигопрогрессировании мРП и являются важной базой для дальнейшего изучения такой методики лечения пациентов в рамках проспективного клинического исследования. А наш молодой пациент за более чем 12-летний период своего лечения продолжал работать без длительных перерывов, растить детей, ездить в отпуск с семьей и жить полной жизнью.
Список литературы: