Новости онкологии Прочти об этом раньше, чем твой пациент
12.03.2024
Длительное время стандартом лечения пациентов с диссеминированным EGFR-мутированным немелкоклеточным раком легкого (НМРЛ) являлось назначение ингибиторов тирозинкиназы I поколения с переходом при прогрессировании заболевания и выявлении мутации T790M на терапию осимертинибом. Перемены произошли в 2020 году, когда публикация положительных результатов исследования FLAURA привела к пересмотру принятых методик и почти вытеснила ингибиторы I поколения из плана лечения у превалирующего числа больных. Однако данный подход не только привел к улучшению отдаленных результатов терапии, но и вновь обозначил следующий вопрос – как же действовать у таких больных при формировании лекарственной резистентности на фоне осимертиниба?
Перспективным направлением лечения данной когорты больных является проведение химиоиммунной терапии в сочетании с бевацизумабом или без него. Теоретико-практические основы подобного подхода были заложены результатами исследований IMPower130 [1] и IMPower150 [2], авторам которого удалось продемонстрировать достоверное улучшение общей выживаемости при добавлении к стандартной платиносодержащей химиотерапии ингибитора контрольных точек. Так, в исследовании IMPower150 медиана ОВ в группах химиоиммунотаргетной (атезолизумаб, бевацизумаб, карбоплатин, паклитаксел) и химиотаргетной терапии (бевацизумаб, карбоплатин, паклитаксел) составили 27,8 и 18,1 мес. соответственно (ОР 0,74; 95% ДИ 0,38-1,46). В то же время улучшение результатов лечения отмечалось лишь в группе одновременного применения атезолизумаба и бевацизумаба, а проведение химиоиммунной терапии без ингибитора VEGF, напротив, демонстрировало тенденцию к снижению выживаемости с медианой ОВ в двух группах 14,9 и 18,1 мес. (ОР 1,22, 95% ДИ 0,68-2,22) (рис.1). Аналогичные результаты были получены и в отношении бессобытийной выживаемости: отношение рисков составило 0,68 для четверной комбинации и 1,55 для химиоиммунной терапии.
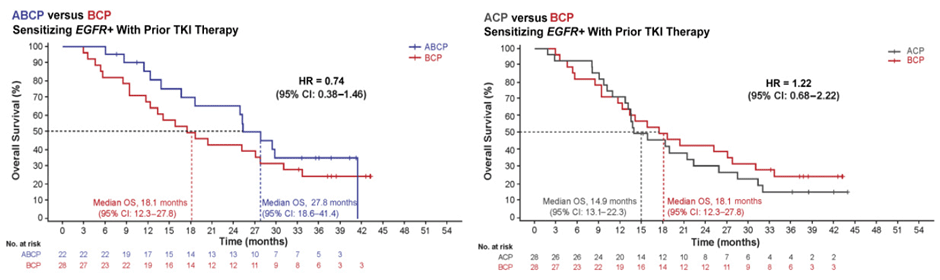
Рисунок 1. Общая выживаемость в исследовании IMPower150.
ABCP – атезолизумаб, бевацизумаб, карбоплатин, паклитаксел; ACP – атезолизукмаб, карбоплатин, паклитаксел; BCP – бевацизумаб, карбоплатин, паклитаксел.
Несмотря на положительные результаты, проведенный в данном исследовании анализ носил эксплоративный характер, а выборка включала всего 78 предлеченных больных с мутацией EGFR, что не позволяет сделать окончательный вывод о всесторонней эффективности подобного подхода и, несомненно, требует дополнительной верификации в дальнейших исследованиях.
Новой попыткой определить оптимальный подход к терапии ≥2 линии стало исследование CheckMate 722 [3], результаты которого были опубликованы в январе 2024 года. Данная работа включила 294 пациента с EGFR-мут. НМРЛ, ранее получивших минимум 1 линию таргетной терапии, а в качестве первичной и вторичной конечных точек были выбраны ВБП и ОВ соответственно. Рандомизация проводилась в группы экспериментальной химиоиммунной терапии (ниволумаб 360 мг, пеметрексед, карбоплатин/
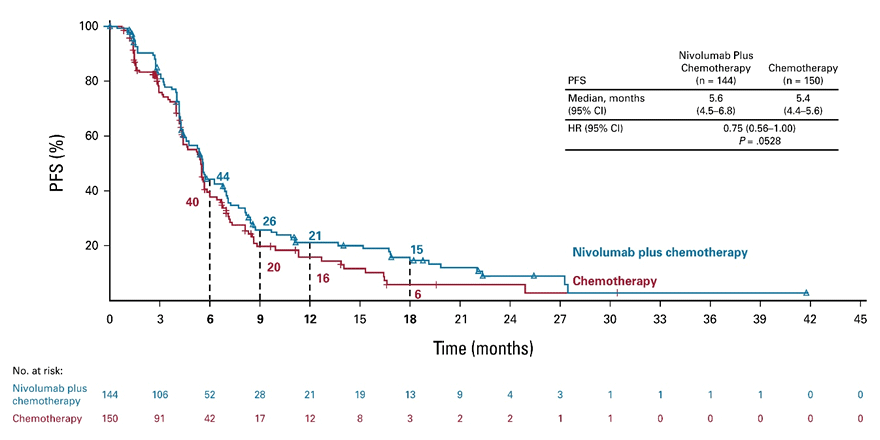
Рисунок 2. Выживаемость без прогрессирования в общей популяции пациентов CheckMate 722.
Проведенный подгрупповой post hoc анализ все-таки выявил когорту больных, потенциально выигрывающих от проведения химиоиммунной терапии, – к ней относились пациенты с наличием чувствительных к классической таргетной терапии мутаций (делеция в 19 экзоне, мутация L858R) (ОР 0,72) и одной линией предшествующей терапии (ОР 0,72). При этом группа больных с двумя характеристиками одновременно демонстрировала наибольшее увеличение ВБП до 6,3 мес. по сравнению с 5,4 мес. в группе контроля (ОР 0,64; 95% ДИ 0,47-0,88) (рис.3), что соотносится с критериями позитивности исследования.
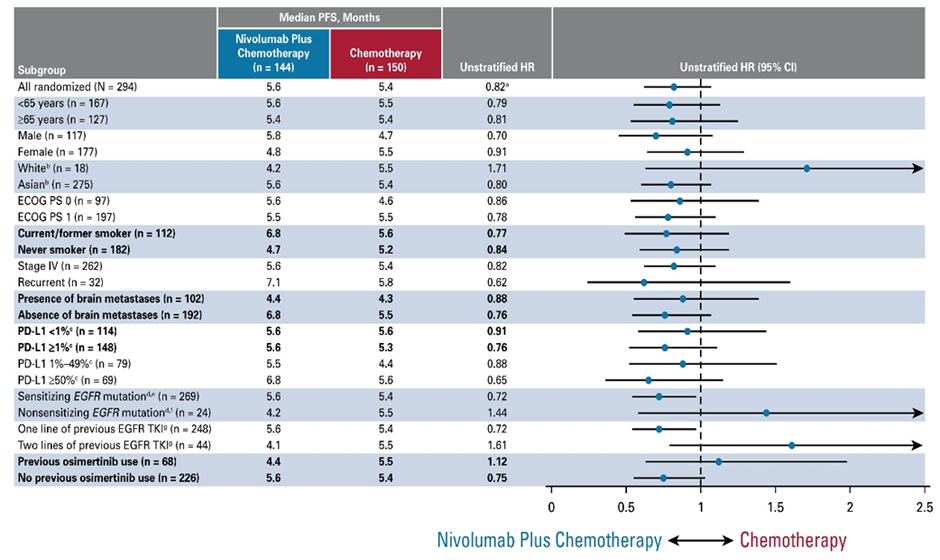
Рисунок 3. Подгрупповой анализ ВБП в CheckMate 722.
Оценка общей выживаемость также не выявила достоверных различий между группами – медиана ОВ в общей популяции составила 19,4 мес. (экспериментальная группа) против 15,9 мес. (контрольная группа) (ОР 0,82) при трехлетних показателях 54% и 46% соответственно. Аналогичные данные были получены при проведении подгруппового анализа.
Таким образом, по результатам данной работы можно заключить, что применение химиоиммунной терапии в общей популяции больных с распространенным EGFR-мут. НМРЛ во ≥2 линии не приводит к увеличению общей или безрецидивной выживаемости по сравнению с платиносодержащей химиотерапией. Однако сами авторы упоминают ряд важных ограничений исследования. Во-первых, превалирующая часть больных не получала осимертиниб ни в 1, ни во 2 линиях терапии, что диссонирует с современной реальной клинической практикой. Во-вторых, данное исследование не включало в протокол лечения ингибиторы VEGF, показавшие высокую эффективность в исследованиях IMPower150 и ORIENT-3 [4]. Возможно, ликвидация данных недочетов позволит в будущем прийти к более обоснованным выводам об эффективности химиоиммунной или химиоиммунотаргетной терапии у данной группы пациентов. Однако на данный момент, по всей видимости, добавление ингибиторов контрольных точек к стандартной химиотерапии не будет приводить к достоверному улучшению отдаленных результатов лечения.
Источники:
Материал подготовил И.М. Боровков