09.02.2024
Трастузумаб эмтанзин компании Roche является первым таргетным препаратом, при применении которого наблюдается значимое увеличение общей выживаемости (ОВ) у пациентов с ранним HER2-положительным раком молочной железы с наличием остаточной инвазивной опухоли после неоадъювантной терапии. Результаты исследования 3-й фазы KATHERINE подтвердили целесообразность применения трастузумаба эмтанзина (торговое наименование «Кадсила»®) в качестве стандартного метода лечения у этой категории пациентов, и к настоящему времени этот препарат получили более 82 000 человек [1].
По данным долгосрочного наблюдения в рамках этого исследования, при применении трастузумаба эмтанзина в качестве адъювантной терапии по сравнению с трастузумабом (торговое наименование «Герцептин»®) наблюдается стабильное улучшение показателей выживаемости без рецидива инвазивного рака молочной железы [1]. Эти данные были представлены в рамках устного доклада на симпозиуме по раку молочной железы в Сан-Антонио в декабре 2023 года.
Компания Roche объявила о положительных результатах долгосрочного наблюдения в рамках базового исследования 3-й фазы KATHERINE с участием пациентов с ранним HER2-положительным раком молочной железы (РМЖ) с наличием остаточной инвазивной опухоли после прохождения неоадъювантной терапии. Статистически достоверное и клинически значимое улучшение ОВ, являющейся дополнительным оценочным показателем, наблюдалось при адъювантной терапии трастузумабом эмтанзином по сравнению с трастузумабом: показатели 7-летней ОВ при применении трастузумаба эмтанзина и трастузумаба составили соответственно 89,07% и 84,37% (отношение рисков [ОР] 0,66; 95% ДИ 0,51-0,87; p=0,0027; рис.1) [1].
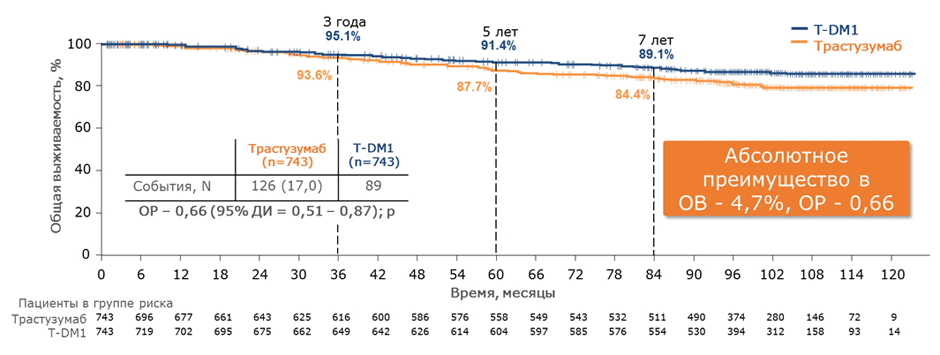
Рисунок 1. Общая выживаемость больных ранним РМЖ с остаточной опухолью после неоадъювантной терапии при применении трастузумаба эмтанзина и трастузумаба.
Также было показано, что полученные ранее результаты по выживаемости без рецидива инвазивного рака молочной железы (основной оцениваемый показатель) сохранялись на прежнем уровне. Применение трастузумаба эмтанзина по сравнению с трастузумабом приводило к снижению риска рецидива заболевания или смерти по любой причине на 46% (ОР 0,54; 95% ДИ 0,44-0,66; p<0,0001), что подтверждает данные первичного анализа, проводившегося в рамках исследования KATHERINE [1,2] (рис.2).
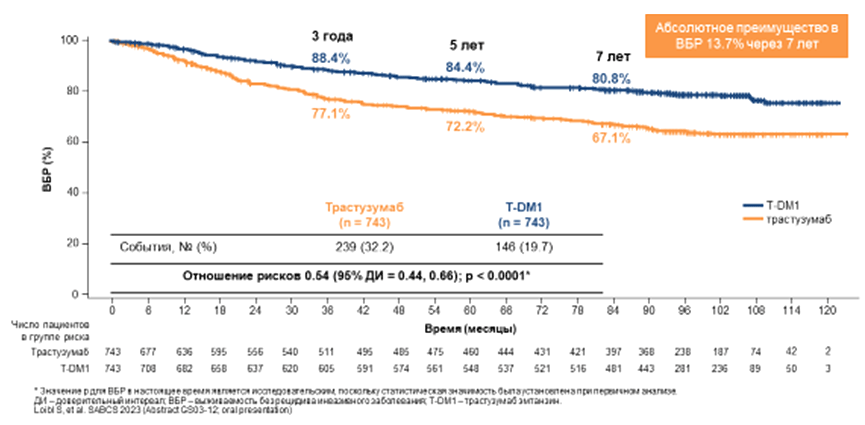
Рисунок 2. Снижение риска рецидива РМЖ у больных с остаточной опухолью при применении трастузумаба эмтанзина и трастузумаба.
Профиль безопасности трастузумаба эмтанзина соответствовал ранее полученным показателям, при этом новых настораживающих нежелательных явлений не отмечалось (рис.3).
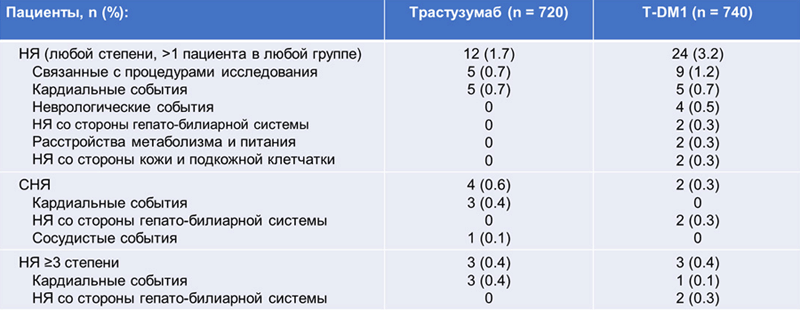
Рисунок 3. Частота нежелательных явлений по завершении терапии трастузумабом эмтанзином и трастузумабом.
«Мы рады, что благодаря трастузумабу эмтанзину у пациентов с ранним HER2-положительным раком молочной железы с особенно неблагоприятным прогнозом появился шанс жить дольше, причем без рецидивов заболевания, – отметил Леви Гаррауэй, доктор медицины, доктор философии, медицинский директор Roche, а также руководитель отдела глобальных разработок лекарственных средств. – Конечной целью лечения рака молочной железы ранней стадии является максимальное повышение шанса на излечение, и полученные результаты свидетельствуют о значительном прогрессе в лечении таких пациентов».
«Благодаря выдающимся достижениям в области диагностики и лечения этого заболевания сейчас больше, чем когда-либо, женщин с первоначальным диагнозом «ранний HER2-положительный рак молочной железы» получили шанс на излечение. Тем не менее, в случае пациентов с заболеванием более высокого риска предотвращение рецидивов и увеличение долгосрочной выживаемости остается непростой задачей, – отметила проф. Сибилла Лойбль, руководитель Немецкой группы изучения рака молочной железы (German Breast Group, GBG), главный исследователь KATHERINE. – Согласно этим новым данным, трастузумаб эмтанзин является первым таргетным препаратом, при применении которого наблюдается значимое увеличение выживаемости у пациентов с ранним HER2-положительным раком молочной железы с наличием остаточной инвазивной опухоли после прохождения неоадъювантной терапии».
Исследование KATHERINE проводилось в сотрудничестве с организациями GBG и NSABP Foundation, Inc. Все данные представлены в рамках устного доклада на симпозиуме по раку молочной железы в Сан-Антонио 8 декабря 2023 г.
Трастузумаб эмтанзин одобрен к применению в 113 странах и является стандартным методом лечения пациентов с ранним HER2-положительным РМЖ с наличием остаточной инвазивной опухоли после прохождения неоадъювантной терапии. Спустя три года у 88,3% пациентов, получавших трастузумаб эмтанзин, не отмечалось рецидивов рака молочной железы, в то время как среди пациентов, получавших трастузумаб, этот показатель составил 77,0%; абсолютное улучшение составило 11,3% [2].
Рак молочной железы является наиболее распространенным типом рака, который оказывает большое влияние на общество [3]. Приблизительно у каждого пятого пациента с раком молочной железы отмечается экспрессия рецепторов человеческого эпидермального фактора роста 2-го типа (HER2), что является особенно агрессивной формой заболевания [4]. Цель лечения раннего РМЖ заключается в том, чтобы предоставить пациентам максимальные шансы на излечение [5-7]. Трастузумаб эмтанзин также одобрен для лечения пациентов с HER2-положительным метастатическим раком молочной железы, которые ранее получали трастузумаб и таксаны.
Информация об исследовании KATHERINE
KATHERINE – это международное многоцентровое рандомизированное открытое исследование 3-й фазы, проводимое с целью сравнительной оценки эффективности и безопасности трастузумаба эмтанзина и трастузумаба в качестве адъювантной терапии у пациентов с ранним HER2-положительным раком молочной железы с наличием остаточной инвазивной опухоли после неоадъювантной терапии с применением трастузумаба и химиотерапии на основе таксанов [8]. В исследовании KATHERINE под остаточной инвазивной опухолью понималось наличие остаточных инвазивных опухолевых клеток в образцах тканей молочной железы и (или) подмышечных лимфатических узлов после проведения неоадъювантной терапии. У пациентов с наличием остаточной инвазивной опухоли после неоадъювантной терапии прогноз обычно хуже, чем у пациентов, у которых при исследовании операционного материала опухолевые клетки не обнаруживаются [9].
Первичной конечной точкой в данном исследовании являлась выживаемость без рецидива инвазивного рака молочной железы, под которой в этом исследовании понимался период времени с момента рандомизации, на протяжении которого не отмечалось рецидивов инвазивного рака молочной железы или смерти по любой причине. К вторичным конечным точкам относились БРВ и ОВ.
Информация о трастузумабе эмтанзине
Трастузумаб эмтанзин представляет собой конъюгат антитела с лекарственным веществом и обеспечивает доставку высокоактивного химиотерапевтического агента непосредственно к HER2-положительным опухолевым клеткам, потенциально ограничивая повреждение здоровых тканей. Он сочетает в себе свойства двух противоопухолевых препаратов, объединенных вместе с помощью стабильного линкера: трастузумаба, который направленно действует на рецепторы HER2, и химиотерапевтического агента DM1 [10]. Трастузумаб эмтанзин одобрен для лечения пациентов с HER2-положительным метастатическим раком молочной железы в 2013 г. и ранним HER2-положительным раком молочной железы в 2019 г. Компания Roche предоставляет разрешение на использование технологий производства трастузумаба эмтанзина в рамках соглашения с компанией ImmunoGen, Inc.
Источники: