01.02.2016

До недавнего времени наш противоопухолевый арсенал был представлен тремя основными методиками: хирургия, лучевая терапия и лекарственное лечение. Кроме этого использовались различные методы абляции, однако они представляли собой методы контактной физической (химической) деструкции локальных опухолевых очагов и идеологически не сильно отличались от хирургии.
Однако в 2012 году совершенно незаметно для широкой онкологической общественности появился новый метод терапии, потенциально претендующий на небольшую революцию в области лечения злокачественных опухолей. Сдержанная реакция онкологов на обнародование первых результатов исследований эффективности и безопасности этого метода была предсказуема, ибо он принципиально отличался от всех ранее известных подходов, а его «теоретическая база» не укладывалась в наше сознание, привыкшее к трем основным доступным методам лечения.
Новый же метод предусматривал использование для лечения злокачественных новообразований низкоинтенсивных переменных электрических полей. В качестве механизма противоопухолевого воздействия, наличие которого было подтверждено в экспериментах in vitro и in vivo, авторы методики называли возможность электрических полей определенной частоты нарушать образование и функционирование веретена деления, а также вызвать направленное смешение внутриклеточных субстратов и органелл [1]. Оба механизма связаны с воздействием электрических полей на внутриклеточные молекулы-диполи (молекулы, имеющие разноименные заряды на полюсах и способные менять ориентацию в пространстве под воздействием электрических полей). За избирательность же действия полей отвечает «правильный» подбор их частоты и интенсивности с учетом опухоли и окружающих ее тканей. Как показали дальнейшие исследования, избирательность метода действительно оказалась на высоте (воздействие практически лишено побочных эффектов, характерных для других видов противоопухолевой терапии) [2], однако первые сообщения о «лечении электричеством» все же были восприняты большинством онкологов скептически.
В качестве первой и до недавнего времени единственной мишени нового метода разработчики выбрали глиобластому – практически всегда фатальную опухоль головного мозга, с очень ограниченным арсеналом доступных лечебных опций. В настоящее время инициальное лечение глиобластомы предполагает максимально возможную циторедукцию с последующей химиолучевой терапией (лучевая терапия до 60 Гр с одновременным применением темозоломида) и адъювантную терапию темозоломидом [3]. Несмотря на то, что по сравнению с отсутствием лечения такой подход позволяет значимо продлить жизнь больных, у подавляющего большинства пациентов он все же не приводит к излечению. По данным различных источников медиана выживаемости больных глиобластомой с момента первоначального диагноза составляет от 12 до 18 месяцев, 5-летняя выживаемость не превышает 10%. При развитии рецидива или нечувствительности к инициальной терапии лечебные опции еще более ограничены – различные режимы химиотерапии, бевацизумаб с или без дополнительного локального лечения (при возможности), обеспечивающие медиану выживаемости, не превышающую 5-9 месяцев. [4, 5].
Для лечения больных рецидивами глиобластомы и было впервые применено устройство, генерирующее «противоопухолевые» электрические поля, получившее название Novo TTF-100А (TTF – tumor treating fields). Устройство (рис. 1, 2) представляет собой носимый генератор электрических полей, соединенный проводами со специальным «шлемом» (состоящим из 12 сменных наружных электродов), который передает поля на зоны воздействия.
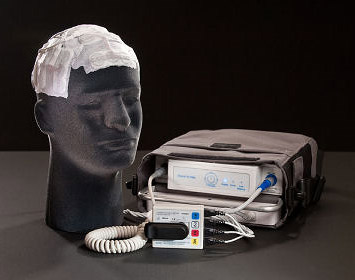

Для обеспечения лечебного эффекта необходимо практически круглосуточное ношение устройства, что позволяет оказать постоянное воздействие на опухоль.
Как ни странно, в отличие от многих устройств, применяемых в онкологии, но использующих более привычный механизм воздействия, перед внедрением в клиническую практику Novo TTF-100А был подвергнут рандомизированным клиническим испытаниям для сравнения с ранее существовавшими методиками. К примеру, различные «сверхновые» устройства и методики для лучевой терапии (протонная терапия, IMRT, IGRT) и хирургии (роботы-хирурги, интраперитонеальная гипертермия и т.д.) при многих заболеваниях были внедрены в клиническую практику без проведения рандомизированных исследований (а иногда даже несмотря на наличие рандомизированных исследований, свидетельствующих об отсутствии преимуществ по сравнению с ранее существовавшими методиками).
В первом исследовании, оценивавшем эффективность и безопасность Novo TTF-100А, были рандомизированы больные с супратенториально расположенным рецидивом или прогрессированием глиобластомы после лечения, в обязательном порядке включавшего лучевую терапию с или без конкурентной/адъювантной химиотерапии. Количество линий предшествующего лечения не ограничивалось. Для включения в исследование больные должны были находиться в относительно удовлетворительном состоянии (индекс Карновского 70 и выше) и не иметь имплантируемых электронных устройств (включая шунты, помпы и т.д.). Пациенты (n=237), отвечающие критериям отбора, были рандомизированы на использование Novo TTF-100А (ежедневно, 22 часа в сутки и более) или терапию по выбору врача. Более 80% больных находились во 2 и более рецидиве заболевания, почти 90% получали темозоломид в процессе химиолучевого лечения и/или адъювантной терапии, 20% ранее получали бевацизумаб. Многие пациенты имели значимый объем опухолевых очагов – медиана наибольшего размера опухоли на момент рандомизации составляла более 5 см. В контрольной группе (терапия по выбору врача) 97% больных в качестве лечения получили химиотерапию (монотерапия или комбинированные режимы).
При медиане наблюдения 36 месяцев результаты лечения в обеих группах оказались практически сопоставимы. Медиана выживаемости без прогрессирования (PFS) больных, использовавших Novo TTF-100А, составила 2,2 против 2,1 месяца в контрольной группе (P=0,16). Медиана общей выживаемости составила 6,6 против 6,0 мес. соответственно (P=0,27). При этом объективные ответы (полная и частичная ремиссия) на лечение чаще наблюдались в группе больных, использовавших Novo TTF-100А – 15% против 9,6% в контрольной группе соответственно. Все три пациента, достигшие полной ремиссии, были из группы Novo TTF-100А.
Терапия с использованием устройства хорошо переносилась, побочные эффекты, ассоциированные с применением Novo TTF-100А, в основном были представлены местным раздражением в области наложения электродов. В то же время, несмотря на тенденцию к улучшению отдельных параметров качества жизни, различия и по этому показателю не достигли статистической значимости. Безусловно, результаты этого исследования нельзя назвать выдающимися в отношении эффективности – оно лишь показало эквивалентность нового метода ранее существовавшему (и, стоит признать, малоэффективному) методу лечения подобных пациентов. Однако эти доказательства были приняты регулирующими органами США: устройство получило одобрение FDA для клинического применения [6] и в качестве возможной лечебной опции было включено в рекомендации уважаемых онкологических сообществ (включено в качестве возможной опции в рекомендации NCCN, хотя и с категорией 2В).
Однако история имела продолжение. В 2014 году на ежегодной конференции нейроонкологов (Society for Neuro-Oncology (SNO) Annual Meeting) были доложены и опубликованы в виде абстракта [7] промежуточные результаты многоцентрового (83 центра из 12 стран) рандомизированного исследования III фазы, оценивавшего эффективность и безопасность использования Novo TTF-100А в качестве компонента стандартной адъювантной терапии глиобластом (параллельно с адъювантным приемом теомозоломида).
Исследование предусматривало, что пациенты после проведения стандартной терапии (максимально возможная циторедуктивная операция, лучевая терапия конкурентно с темозоломидом) будут рандомизированно распределяться (2:1) на получение адъювантной терапии темозоломидом с или без одновременного использования NovoTTF-105А. Первичной целью исследования была выживаемость без прогрессирования, вторичной – общая выживаемость. Критерии отбора подразумевали наличие гистологически подтвержденного диагноза глиобластомы (по классификации ВОЗ), возраст старше 18 лет, проведение адекватного предшествующего лечения, статус Карновского 70% и выше, предполагаемую продолжительность жизни как минимум 3 месяца. Доза кортикостероидов, принимаемых пациентами, должна была быть стабильна или уменьшаться перед включением, время, прошедшее с момента окончания лучевой терапии, должно было быть >29, но <49 дней.
Характеристики пациентов были сопоставимы между собой – средний возраст составил 57 и 58 лет для группы комбинированной терапии и монотерапии темозоломидом, выраженность циторедуктивной хирургии составила 89% и 90% соответственно. У 60% больных в обеих группах был определен статус метилирования промотора MGMT, который оказался метилирован у 39% и 41% больных соответственно.
Исследование было приостановлено в силу явного преимущества экспериментальной группы после первого запланированного промежуточного анализа результатов лечения первых 315 включенных пациентов (210 в группе с использованием комбинированной адъювантной терапии и 105 в группе монотерапии темозоломидом), наблюдавшихся на протяжении не менее 18 месяцев. Медиана выживаемости без прогрессирования составила 7,1 мес. в группе комбинированной терапии против 4,0 мес. в группе монотерапии теомозоломидом (HR=0,63; P=0,001). Медиана общей выживаемости составила 19,6 против 16,6 мес. соответственно (HR=0,75; P=0,034). Двухлетняя выживаемость была 43% в группе комбинированной терапии против 29% у больных, получавших только темозоломид. Наиболее частым нежелательным явлением от использования NovoTTF-105А было раздражение кожи в области контакта с электродами, встречавшееся у 45% больных, но имевшее умеренный характер у подавляющего большинства из них. В последующем результаты исследования были доложены на конференции ASCO 2015, вновь опубликованы в виде абстракта и, наконец, в виде статьи в высокорейтинговом журнале американской медицинской ассоциации JAMA [8]. На момент подачи статьи медиана наблюдения за больными составляла 18 месяцев. Медиана выживаемости без прогрессирования, кривые выживаемости, представленные в статье, выглядят достаточно впечатляюще с учетом заболевания, о котором идет речь (рис. 3).
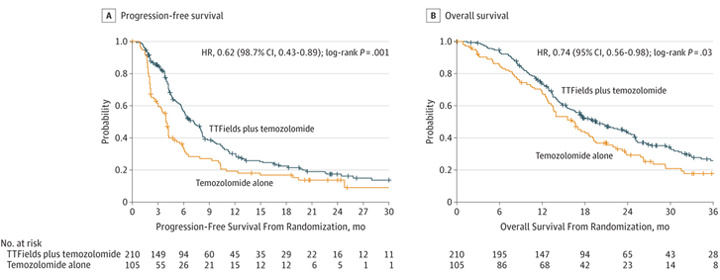
Несмотря на ряд сомнений, например, отсутствие ослепления в дизайне обоих исследований, потенциальном конфликте интересов – ряд исследователей являются акционерами компании, владеющей NovoTTF-105А, и по-прежнему неоднозначной оценке данного подхода рядом зарубежных экспертов, данная тема показалась нам крайне интересной и заслуживающей изложения. Тем более что еще в 2012 компания анонсировала начало и проведение исследования в области лечения других злокачественных опухолей.
И вот к моменту, когда заметка была уже почти готова, но оставались сомнения в целесообразности ее публикации, появилось сообщение о потенциальной эффективности устройства для лечения больных раком поджелудочной железы. В небольшом исследовании PANOVA, включившем 20 больных местно-распространенным, нерезектабельным или метастатическим раком поджелудочной железы, устройство использовалось одновременно с еженедельными введениями гемцитабина в стандартном для данного заболевания режиме (1250 мг/м2, еженедельно, 7 недель, затем 1, 8 и 15 дни каждые 28 дней). На фоне проводимой терапии у 30% больных было отмечено достижение частичной регрессии, еще у 30% – стабилизации процесса, медиана выживаемости без прогрессирования составила 8,3 мес., общей выживаемости 14,9 мес., год и более прожили 53% больных [9]. При непрямом сравнении эти данные выглядят гораздо более многообещающими, чем результаты использования гемцитабина в одном из современных исследований III фазы при раке поджелудочной железы, где медиана выживаемости без прогрессирования составила 3,7 мес., общей выживаемости – 6,7 мес., а один год пережили лишь 22% больных [10].
Безусловно, в отношении рака поджелудочной железы это лишь очень предварительные данные, но все же, как нам кажется, уже сейчас можно с уверенностью сказать, что в ближайшее время в руках онкологов возможно появится принципиально отличный от всех ранее существовавших метод лечения злокачественных новообразований. И дальше стыдливо обходить молчанием эту тему, пожалуй, не стоит, даже если мы не совсем понимаем, как работает данный вид терапии.
Литература: