
Каждый год открываются новые горизонты возможностей борьбы со злокачественными новообразованиями. Так как ежегодно публикуются результаты сотен клинических исследований, важной задачей становится выявление наиболее значимых открытий. Шесть лет назад для решения этой проблемы ASCO стало публиковать обзорные статьи под названием «Успехи клинической онкологии».
В публикации ASCO упоминаются лишь работы, значительно повлиявшие на понимание рака или имевшие непосредственное влияние на тактику лечения больных, выбранные редакционной коллегией, собранной под руководством четырнадцати крупных американских онкологов. Редакторы, в том числе редакторы отдельных разделов доклада, производили обзор исследований, представленных на крупных научных мероприятиях или опубликованных в рецензируемых журналах в период с октября 2009 г. по сентябрь 2010 г. JCO December 20, 2010 vol. 28 no. 36 5327-5347.
В этом номере газеты мы приводим обзор наиболее значимых событий по мнению экспертов ASCO и ESMO
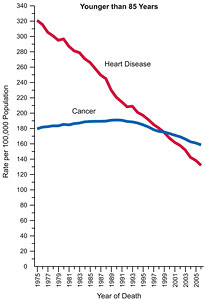
Несмотря на снижение смертности от злокачественных новообразо- ваний, темпы снижения являются недостаточными. По данному показателю злокачественные опухоли существенно уступают сердечно-сосудистым болезням. Jemal A. et al. CA Cancer
J Clin 2010; 60:277-300.
В докладе, опубликованном в конце 2009 г. ведущими медицинскими и онкологическими организациями США, было показано, что за последние годы количество вновь выявленных больных и суммарное количество смертей от всех злокачественных новообразований значительно уменьшилось в большинстве расовых и этнических популяций США.
Доклад, выпущенный NCI, центрами по контролю и предотвращению заболеваний США, Американским обществом по борьбе с раком (American Cancer Society) и североамериканской ассоциацией центральных раковых регистров, показал, что количество регистрируемых новых случаев рака снижалось в среднем на 1% в год между 1999 и 2006 г. Кроме того, с 2001 по 2006 г. число смертей от рака снижалось ежегодно на 1,6%, что во многом было обусловлено снижением заболеваемости и смертности по трем наиболее распространенным злокачественным новообразованиям у мужчин (рак легкого, предстательной железы и колоректальный рак) и двум из трех наиболее распространенных видов рака у женщин (рак легкого и колоректальный рак).
На фоне общего снижения смертности от злокачественных новообразований в РФ существуют опухоли, для которых наблюдается неблагоприятная динамика по данному показателю. Например, к ним относится рак почки. Так, прирост общего количества смертей от заболевания за 2001-2008 годы составил 14,4 и 7,8% у мужчин и женщин. При этом та же тенденция отмечена при оценке стандартизованных показателей – 14,8 и 4,8%. При сравнении медианы выживаемости в исследовании по типу «случай-контроль» в хорошо сбалансированных группах по всем стадиям за 1999-2002 гг. и 2003-2006 гг. достоверных отличий не было (P=0,168). Общая 5-летняя выживаемость за 2001-2005 годы составила 59,7%, что приблизительно на 10% меньше по сравнению с США и Великобританией и соответствует северным странам (например, Финляндии).
Tsimafeyeu I, Aksel E. Renal Cell Carcinoma in the Russian Federation in 2008.
Malign Tumours 2010;1:1-4.
 На пресс-конференции, прошедший накануне Международного дня борьбы с раком, Валерий Иванович Чиссов сообщил: «Благодаря реали- зации Нацпроекта «Здоровье» в прошлом году смертность от онкологических заболеваний в России впервые сократилась на 0,3%».
На пресс-конференции, прошедший накануне Международного дня борьбы с раком, Валерий Иванович Чиссов сообщил: «Благодаря реали- зации Нацпроекта «Здоровье» в прошлом году смертность от онкологических заболеваний в России впервые сократилась на 0,3%».
Профессор Чиссов рассказал, что благодаря массовому скринингу в последние годы наблюдается рост выявляемости онкологических заболеваний на ранних стадиях, когда шансы на спасение жизни человека значительно выше. «Если больной приходит к нам на первой или второй стадии мы достигаем в 90-95% случаев положительного результата. Также важно, что на более ранней стадии человек обращается за помощью к онкологу, тем ниже вероятность рецидива развития опухоли», – объяснил академик. Он подчеркнул, что для снижения смертности от онкологических заболеваний в России достаточно онкологической настороженности врача и личной ответственности человека: чем раньше будет выявлено заболевание в ходе профилактического обследования.
Валерий Чиссов отметил, что меры, заложенные в нацпроекте «Здоровье» сегодня позволяют закупать новейшее оборудование, необходимое как для диагностики, так и лечения больных с онкологией. Также он отметил, что важно не только финансирование. «Главное подготовка кадров и создание системы следования больного от первичного обследования до дальнейшего лечения, – пояснил Валерий Чиссов. – Сегодня кафедры онкологии усиливаются, они объединяются с кафедрами радиологии».
Он также объяснил, что существую четкие порядки оказания помощи онкологическим больным, описанные в приказах Минздравсоцразвития России.
Особо Валерий Чиссов отметил, что сегодня развивается сеть специализи-рованных онкодиспансеров. Он сказал, что это особенно важно, так «онкологический больной должен лечиться у онколога, располагающего полным спектром необходимых методов». В ближайшее время планируется открытия нового онкологического центра в Красноярске, в следующем году планируется открыть центр в Татарстане.
В ходе пресс-конференции были продемонстрированы достижения российских врачей онкологов. В частности, молодой человек (29 лет), которому в декабре 2009 года удалили 2,5 позвонка, пораженных злокачественной опухолью, на глазах собравшихся продемонстрировал полное сохранение двигательной активности. По словам врачей в ближайшие две недели он будет готов к выписке.
Заведующий отделением онкологической ортопедии НИИ им. Герцена Валерий Тепляков отметил, что сегодня российские врачи в 90% случаев злокачественных заболеваний опорно-двигательного аппарата удается обойтись без ампутации. Валерий Чиссов рассказал, что все эти операции проводятся за счет бюджетных средств, поскольку «Минздравсоцразвития России отдельной статьей выделило финансирование эндопротезирования».
3 февраля 2011 г.,
официальный интернет-сайт Минздравсоцразвития России
Некоторые опухоли редко выявляются на ранних стадиях и чаще диагностируются запущенными, и многие из них обладают врожденной резистентностью к химиотерапии. Достижения в лечении этих тяжело поддающихся лечению опухолей приводятся далее.
Полихимиотерапия увеличивает выживаемость пожилых больных распространенным раком легкого
Комбинация карбоплатина и паклитаксела, являющаяся стандартом для лечения молодых больных раком легкого, увеличивает выживаемость пожилых больных в сравнении с монотерапией гемцитабином или винорельбином. Хотя пожилые больные часто получают менее агрессивное лечение, авторы мультицентрического исследования III фазы сообщили, что более агрессивная терапия показала большую эффективность и хорошую переносимость у этой группы больных.
Полихимиотерапия существенно увеличивает выживаемость больных метастатическим раком поджелудочной железы
Рандомизированное исследование III фазы было, насколько нам известно, первой работой, показавшей существенное увеличение выживаемости больных IV стадией аденокарциномы поджелудочной железы. Авторы установили, что применение комбинации 5-фторурацила, лейковорина, иринотекана и оксалиплатина (FOLFIRINOX) увеличило показатели общего ответа, выживаемости без прогрессирования и общей выживаемости в сравнении со стандартной монотерапией гемцитабином (Gemzar; Lilly, Индианаполис, Индиана).
Бевацизумаб увеличивает выживаемость без прогрессирования у женщин с распространенным раком яичников
В исследовании III фазы было показано, что добавление антиангиогенного препарата бевацизумаба, блокирующего рост и развитие кровеносных сосудов в опухоли, к стандартной комбинации карбоплатина и паклитаксела продлило выживаемость без прогрессирования женщин, больных распространенным раком яичников, в сравнении с женщинами, получавшими только химиотерапию. В исследование были включены больные эпителиальным раком яичников, первичным перитонеальным раком яичников и раком фаллопиевой трубы. Исследователями было продемонстрировано, что бевацизумаб в добавление к химиотерапии с последующим длительным лечением бевацизумабом является наиболее эффективной терапевтической стратегией.
Ипилимумаб увеличивает выживаемость при диссеминированной меланоме
Первое, по нашим сведениям, рандомизированное исследование III фазы, показавшее увеличение выживаемости больных диссеминированной меланомой. Исследователи показали, что применение экспериментальной иммунотерапии ипилимумабом – человеческим моноклональным антителом, поддерживающим активность Т-клеток иммунной системы, в том числе тех, мишенью которых являются клетки меланомы, – увеличило 2-летнюю выживаемость больных на 34%. Также сообщалось об увеличении контроля над болезнью в течение 6 месяцев почти до 30% в сравнении с 11% в группе контроля.
Уменьшение частоты рецидивов
Хотя многие виды злокачественных новообразований на первом этапе успешно поддаются лечению, тяжелой проблемой остается борьба с возвратом заболевания. Рецидивные опухоли часто характеризуются резистентностью к лечению и приводят к смерти больных. В прошлом году были отмечены важные успехи в решении проблемы рецидивов при раке молочной железы: было показано, что сокращение продолжительности курсов лучевой терапии при раке молочной железы не уменьшает эффективности профилактики рецидивов при ранних стадиях рака молочной железы. Гипофракционированная терапия, представляющая собой короткие трехнедельные курсы лучевой терапии более высокими дозами, обладала такой же эффективностью, как и стандартные курсы продолжительностью пять недель у женщин, больных ранними стадиями рака молочной железы. Риск развития локальных рецидивов через 10 лет в двух группах, состоящих из более чем шестисот женщин, рандомизированно получавших короткие или стандартные курсы лучевой терапии, был почти одинаковым.
Таргетная терапия и индивидуальный выбор лечения
По мере накопления знаний о биологии и течении злокачественных новообразований ученые добиваются успехов в развитии лечебных подходов, направленных на индивидуальный подбор терапии на основании генетических особенностей отдельных опухолей и больных. Далее представлены основные достижения в области индивидуализации лечения и таргетной терапии, опубликованные в минувшем году.
Высокий уровень ответа на лечение новым ингибитором ALK в группе больных раком легкого
Исследование I фазы показало, что более чем у двух третей больных с мутацией гена ALK (около 5% больных раком легкого) отмечалось сокращение объема опухолевой массы при лечении ингибитором ALK кризотинибом. Целью исследований I фазы обычно является оценка токсичности, в них редко достигается выраженная клиническая активность препарата. На лечение данным препаратом ответило более 90% из 82 включенных в исследование больных: у части наблюдалось прекращение роста опухоли, у остальных – уменьшение опухоли.
Обнадеживающие результаты новой таргетной терапии у больных распространенной меланомой с мутацией гена BRAF
В исследовании, дающем надежду на перспективы применения таргетного лечения при меланоме, было показано, что большинство больных распространенной меланомой со специфической мутацией гена BRAF (мутация V600E) отвечает на лечение новым ингибитором BRAF PLX4032. Во второй части исследования I фазы частичная или полная регрессия опухоли, в том числе метастазов в кости и печень, отмечалась у 81% больных.
Несколько важных исследований этого года было посвящено улучшению качества жизни больных злокачественными новообразованиями.
Добавление паллиативного лечения к химиотерапии повышает выживаемость больных раком легкого
Рандомизированное клиническое исследование, в которое были включены больные распространенным раком легкого, показало, что пациенты, получавшие стандартную химиотерапию в комбинации с паллиативным лечением непосредственно после постановки диагноза, жили значимо дольше и имели лучшее качество жизни в сравнении с пациентами, получавшими только химиотерапию. Больные, регулярно встречавшиеся со специалистами по паллиативной помощи, реже испытывали депрессию и боли, были более подвижны и реже получали в конце жизни неэффективное и агрессивное лечение, чем больные, получавшие только химиотерапию. Исследование получило награду Career Development Award от фонда ASCO Cancer Foundation.
Проблемы со сном влияют на состояние большинства больных злокачественными новообразованиями, получающих химиотерапию
По нашим сведениям, это было первое исследование, изучавшее распространение бессонницы у больных, получающих химиотерапию. Исследователи показали, что более чем три четверти химиотерапевтических больных страдают от бессонницы и других нарушений сна, что почти в три раза превышает распространенность этой проблемы в общей популяции. Также было установлено, что проблемы со сном чаще наблюдались у пациентов моложе 58 лет, и что больные, страдающие бессонницей, значимо чаще предъявляли жалобы на депрессию и повышенную утомляемость, чем больные без нарушений сна.
 В январе 2011 года была создана рабочая группа Российского общества клинической онкологии по диагностике и лечению меланомы. Группу возглавил руководитель Российского Экспертного Совета по Меланоме Международного Комитета Global Melanoma Task Force, заведующий отделением биотерапии опухолей ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, профессор Демидов Лев Вадимович.
В январе 2011 года была создана рабочая группа Российского общества клинической онкологии по диагностике и лечению меланомы. Группу возглавил руководитель Российского Экспертного Совета по Меланоме Международного Комитета Global Melanoma Task Force, заведующий отделением биотерапии опухолей ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, профессор Демидов Лев Вадимович.
Сообщение общества медицинской онкологии (ESMO)
В связи с наступлением нового 2011 года Европейское общество медицинской онкологии (ESMO) также подвело свои итоги года ушедшего. Они назвали три сообщения, опубликованных на сайте ESMO в разделе «новости науки», которые имели больше всего посещений и нашли наибольший отклик в 2010 году.
Трастузумаб был первым новейшим биологическим противоопухолевым препаратом, доступным для клинического применения при солидных опухолях. Исходные данные не были многообещающими. Общий ответ при монотерапии трастузумабом тяжело предлеченных больных HER2-позитивным метастатическим раком молочной железы составил не более 11,6%, и на тот момент было очень мало известно о биологической и клинической роли HER2 как важнейшей терапевтической мишени при раке молочной железы. Возможности трастузумаба стали открываться при добавлении препарата к химиотерапии первой линии, но на тот момент еще не были опубликованы данные исследований III фазы, сравнивающих два или более трастузумаб-содержащих режима лечения в первой линии. В дальнейшем, после утверждения применения трастузумаба в качестве адъювантной терапии при HER2-позитивном раннем раке молочной железы в 2006 г. трастузумаб стал первым моноклональным антителом, рекомендованным для применения в качестве адъювантной терапии при злокачественных новообразованиях.
Вскоре начала поступать новая информация, касавшаяся трастузумаба. В частности, наметилась тенденция к применению трастузумаба после прогрессирования у больных, получавших таксан-содержащую химиотерапию. Для решения этого вопроса помимо одного опубликованного проспективного исследования между 2004 г. и 2007 г. в США и Европе было зарегистрировано не менее пяти рандомизированных мультицентрических исследования (три исследования III фазы и два II фазы). Ни одно из них не завершило запланированный набор больных, четыре из них были приостановлены из-за слишком медленного набора больных и/или изменений, последовавших в представлении о второй линии лечения HER2-позитивного рака молочной железы.
Ситуация осложнилась еще больше после внедрения в клиническую практику двойного ингибитора тирозинкиназ (HER-1 и HER-2) лапатиниба. До сегодняшнего дня не было исследования, которое бы сравнивало применение трастузумаба с химиотерапией лапатинибом и капецитабином во второй линии лечения. Учитывая, что исследование комбинации лапатиниба и капецитабина было достаточно мощным, представляется разумным рассматривать эту схему в качестве возможного стандарта второй линии терапии HER2-позитивного рака молочной железы. Однако практика продолжения применения трастузумаба с другим цитотоксическим препаратом коснулась третьей и последующих линий лечения, при которых практически полностью отсутствуют данные об эффективности и безопасности. Основную роль в ответе на лечение ингбиторами HER2 у больных, получавших ранее несколько линий трастузумаба, могут играть молекулярные механизмы резистентности.
Так как рутинное использование трастузумаба для лечения рецидивных или резистентных опухолей приведет к применению препарата у очень большого количества больных, важнейшим вопросом остается экономическая эффективность этого метода лечения. Единственным на сегодня исследованием, касающимся этого аспекта применения трастузумаба, является анализ, произведенный Matter-Walstra и опубликованный в 2010 г. в журнале «Annals of Oncology». В этой работе был выполнен анализ полезности затрат при применении трастузумаба в комбинации с капецитабином во второй линии лечения HER2-позитивного метастатического рака молочной железы.
Клинические данные для этого анализа были взяты из исследования GBG26/BIG03-05 (von Minckewitz et al.), единственного опубликованного проспективного исследования у этой группы больных, но тоже обладавшего рядом ограничений. Во-первых, за 4 года, что почти вдвое превышало запланированный срок набора больных, в исследование было включено лишь 32% от запланированного количества пациенток. Во-вторых, ответ на лечение оценивался не независимо, что повышает вероятность необъективности результатов. Наконец, необходимо принять во внимание, что в анализе Matter-Walstra медицинские затраты оценивались на основании работы Швейцарской медицинской системы и непрямые расходы на лечение не принимались во внимание. Тем не менее, эта работа представляет собой достаточно точный и всесторонний анализ, принимающий во внимание все наиболее значимые параметры и применяющий необходимые статистические методы.
Авторами было показано, что применение трастузумаба и капецитабина при прогрессировании после трастузумабсодержащей терапии первой линии не укладывается в рамки того, что обычно расценивается как экономическая эффективность. Было показано, что, как и ожидалось, основной причиной дополнительных расходов явилось применение трастузумаба, и лишь малую часть из них взяли на себя побочные эффекты лечения. Авторами было посчитано, что при снижении стоимости трастузумаба на 30–60% ситуация изменится и стоимость этого вида лечения с гораздо большей вероятностью может войти в те границы, в которых оно может быть оплачено. Несмотря на низкую экономическую эффективность данного режима, при сравнении с некоторыми другими режимами, ставшими стандартом лечения в последние годы, например с химиотерапией таксанами плюс бевацизумаб в первой линии при распространенном HER2-негативном раке молочной железы, неожиданно экономическая эффективность применения трастузумаба во второй линии оказалась выше.
Важно также отметить, что добавление лапатиниба к капецитабину у той же группы больных также не эффективнос экономической точки зрения. Также необходимо учитывать, что в большинстве стран Европы не установлены формальные границы экономической эффективности лечения.
В заключение нужно признать, что через 12 лет после регистрации трастузумаба для лечения рака молочной железы и после многих установленных им рекордов остается большое количество вопросов по оптимизации клинического применения этого препарата. Например, комбинация трастузумаба с капецитабином не основана на каких-либо преклинических или предварительных данных и несмотря на все попытки установить какие-либо дополнительные молекулярные маркеры, способные предсказать первичную или приобретенную резистентность к трастузумабу, до сих пор в клинической практике не применяется никаких исследований, кроме определения гиперэкспрессии или амплификации HER2.
В крупном рандомизированном исследовании OVA-301 было показано преимущество применения комбинации трабектедина и пегилированного липосомального доксорубицина (ПЛД) перед монотерапией ПЛД при рецидивах рака яичников.
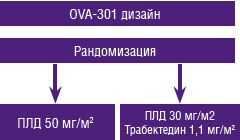 На сегодняшний день оптимальный режим лечения больных частично платиночувствитель- ными рецидивами рака яичников, то есть больных с бесплатиновым интервалом (БПИ) от 6 до 12 месяцев, остается неопределенным. В рамках исследования OVA-301 группа исследователей под руководством доктора A. Poveda из института Instituto Valenciano de Oncologia, Валенсия, Испания изучила результаты лечения 214 больных этой популяции.
На сегодняшний день оптимальный режим лечения больных частично платиночувствитель- ными рецидивами рака яичников, то есть больных с бесплатиновым интервалом (БПИ) от 6 до 12 месяцев, остается неопределенным. В рамках исследования OVA-301 группа исследователей под руководством доктора A. Poveda из института Instituto Valenciano de Oncologia, Валенсия, Испания изучила результаты лечения 214 больных этой популяции.
Применение комбинации трабектедина и ПЛД снизило риск прогрессирования заболевания или смерти на 35% (относительный риск [ОР] 65%, 95% доверительный интервал [ДИ] 0,45–0,92, p=0,0152; медиана выживаемости без прогрессирования [ВБП] 7,4 vs 5,5 месяцев) и риск смерти на 41% (ОР 0,59; 95% ДИ 0,43–0,82; p=0,0015; медиана общей выживаемости 23,0 vs 17,1 месяцев).
Переносимость лечения у больных, получавших данную схему лечения, не отличалась от таковой в общей популяции. Одинаковая доля больных в обеих группах получала дальнейшее лечение (76% vs 77%), хотя больные группы трабектедина+ПЛД реже получали препараты платины (49% vs 55%). Важно заметить, что выживаемость больных группы трабектедин+ПЛД после последующего лечения платиносодержащими схемами была значимо выше (ОР 0,63; p = 0,0357; медиана выживаемости 13,3 vs 9,8 месяцев).
Данные о результатах лечения частично платиночувствительных больных в рамках исследования OVA-301 были опубликованы в журнале «Annals of oncology» и вызвали широкое обсуждение в контексте данных других рандомизированных исследований III фазы платиночувствительных рецидивов рака яичников. В исследование OVA-301 вошло 35% больных платинорезистентным раком яичников, в то время как другие исследования включали только больных, чувствительных к препаратам платины. В исследовании CALYPSO, выполненном группой ученых в рамках Gynecologic Cancer Intergroup, было произведено сравнение комбинации карбоплатин + ПЛД и комбинации карбоплатин + паклитаксел, и были отдельно показаны результаты лечения больных частично платиночувствительными рецидивами. В данной популяции также была показана более высокая ВБП при применении комбинации с ПЛД (снижение риска прогрессирования или смерти на 27%; медиана ВБП 9,4 vs 8,8 месяцев).
Было отмечено, что при анализе данных исследования OVA-301 применялись очень точные и жесткие методы. Первичная диагностика у больных с измеряемым объемом поражения выполнялась независимой группой радиологов, не имевшей информации о группе лечения больных. Для оценки результатов также в слепом режиме выполнялся независимый пересмотр данных, сравнивавший данные радиологических методов исследования с результатами лечения.
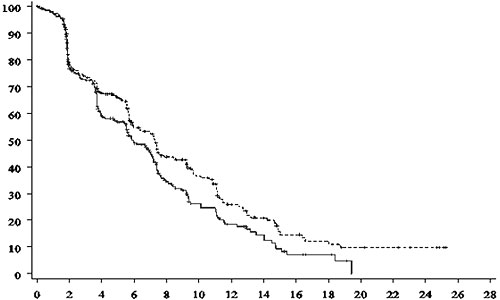
Рисунок. Выживаемость без прогрессирования
Исследование OVA-301 подтвердило преимущество комбинации трабектедина и ПЛД в сравнении с монотерапией ПЛД и показало, что наилучшие результаты достигаются в популяции больных частично платиночувствительным раком яичников. Так как большинство женщин с рецидивом рака яичников в конечном итоге ожидает прогрессирование заболевания и смерть от него, в оценке места новой схемы лечения этой популяции больных важнейшую роль играет и эффективность лечения, и его безопасность. Применение схемы лечения, не содержащей препараты платины, может предоставить возможность его проведения больным, еще не восстановившимся от предшествовавшей токсичности (в том числе резидуальная нейротоксичность или гиперчувствительность) и, как было показано в субпопуляции частично платиночувствительных больных в исследовании OVA-301, может улучшить результаты последующего лечения препаратами платины. Кроме того, существуют данные о возможности замены карбоплатина на трабектедин у больных с гиперчувствительностью к карбоплатину, что делает необходимым проведение рандомизированного исследования с косвенными и трансляционными оцениваемыми показателями, сравнивающего применение этих препаратов в одной популяции.
Авторы делают вывод, что комбинация трабектедина и ПЛД является новой терапевтической опцией для больных с рецидивом рака яичников после неудачи терапии первой линии препаратами платины. Поскольку в этой популяции больных возможно возобновление лечения платиносодержацими режимами, необходимы дальнейшие исследования для сравнения трабектедина + ПЛД с режимами, содержащими препараты платины. В настоящее время готовится исследование для оценки общей выживаемости больных частично платиночувствительными рецидивами рака яичника, получающих лечение по схеме трабектедин + ПЛД (с последующим лечением препаратами платины) или по схеме карбоплатин + ПЛД, недавно изученной в исследовании CALYPSO.
Таким образом, рандомизированное исследование III фазы OVA-301 показало, что применение трабектедина в комбинации с ПЛД дает удовлетворительные показатели ВБП и общей выживаемости и представляет собой эффективную и безопасную альтернативу для лечения больных рецидивным платиночувствительным раком яичников, не содержащую препараты платины или таксаны. Данные, полученные при анализе результатов лечения больных с частично платиночувствительными рецидивами (БПИ 6–12 месяцев), показывают высокую эффективность схемы трабектедин + ПЛД для этой популяции больных. Данный режим лечения может применяться при рецидивах рака яичников для одновременно с купированием побочных эффектов препаратов платины, и удлинение БПИ может позволить увеличить ответ на последующее лечение препаратами платины и, в дальнейшем, выживаемость.
Концепция повторного применения терапии первой линии для лечения поздних рецидивов встречается в онкологии не впервые. Эта тактика применяется в лечении рака яичников, лимфомы Ходжкина, немелкоклеточного и мелкоклеточного рака легкого. Адъювантная терапия комбинацией антрациклинов и таксанов является общепринятой стратегией лечения ранних стадий рака молочной железы высокого риска. После начала новой эры в лечении этого заболевания, в которой лечение антрациклинами и таксанами рака молочной железы высокого риска стало повсеместным, при этом кумулятивные дозы антрациклинов ниже предельных для развития кардиотоксичности, а длительность применения и дозы таксанов ниже, чем используются обычно, встал вопрос о возможном изучении применения этих препаратов повторно при развитии отдаленных рецидивов рака молочной железы. Данные о применении этой стратегии были изучены в обзорной статье, опубликованной 31 августа 2010 г. доктором Carlo Palmieri и доктором Jonathan Krell из Imperial College, Лондон, в журнале Nature Reviews Clinical Oncology.
Авторы сообщили, что на сегодняшний день данные о повторном применении обоих классов препаратов при отдаленных рецидивах рака молочной железы немногочисленны и в основном представляют собой данные одноцентровых когортных исследований, небольших исследований II фазы или анализы подгрупп или ретроспективные обзоры исследований III фазы. Проблемой часто является определение и измерение ответа на лечение, центральный пересмотр в большинстве случаев не применяется. Лишь в одном исследовании III фазы сообщалось об эффективности повторного применения антрациклинов. Более того, до сегодняшнего дня не было проведено ни одного сравнительного проспективного исследования повторного применения антрациклинов или таксанов для лечения больных, получавших препараты обеих групп в качестве адъювантной терапии.
Для сравнения с таксанами липосомальные формы антрациклинов могут быть предпочтительнее стандартных ввиду меньшей кардиотоксичности, особенно принимая во внимание повреждение миокарда, которое могло развиться у больных при предшествовавшем применении антрациклинов. Было проведено одно исследование, сравнивавшее применение комбинации пегилированного липосомального доксорубицина и доцетаксела с монотерапией доцетакселом. При выборе препарата для повторного применения таксанов открывается несколько вариантов, например другой представитель класса, альтернативный режим с тем же препаратом или применение иной формы препарата, например связанный с альбумином паклитаксел.
Недавнее изучение регистра клинических исследований Национальных институтов здоровья показали, что в настоящее время проводится большое количество исследований эффективности применения доцетаксела у больных метастатическим раком молочной железы, но диапазон возможной предшествующей длительности получения таксанов очень широк (от 6 до 12 месяцев). Очевидно, что предположение об эффективности повторного применения таксанов в этих исследованиях сделано вопреки отсутствию данных рандомизированных проспективных исследований, подтверждающих эту гипотезу. Это может обесценить данные этих работ, что особенно важно при исследовании комбинации таргетных препаратов с таксанами. На сегодняшний день нет достоверных данных о применении других режимов лечения, не содержащих антрациклины и таксаны, позволяющих однозначно рекомендовать какую-либо схему лечения больных с рецидивом рака молочной железы после стандартной адъювантной терапии.
Авторы предупреждают, что при нивелировании значения ранее применявшихся препаратов из-за появления новых арсенал средств для лечения рецидивного рака молочной железы может быть уменьшен, и возможности повторного применения препаратов могут быть недооценены. Более того, так как антрациклины и таксаны являются наиболее эффективными препаратами для лечения рака молочной железы, кажется вероятным, что при реализации стратегии их повторного применения они должны использоваться в первом рецидиве, а не позднее. Однако вопрос о повторном применении того же препарата или о замене на другой препарат той же группы остается открытым.
Авторы приходят к выводу, что на сегодняшний день мы обладаем очень скудными данными о возможности повторного применения препаратов при рецидивах рака молочной железы. Чтобы определить, является ли повторное применение антрациклинов и/или таксанов правильной тактикой лечения отдаленных рецидивов рака молочной железы, необходимы проспективные рандомизированные исследования. Они также крайне важны для определения химиотерапевтического «каркаса», в комбинации с которым могут исследоваться новые биологические препараты.
 Н.В. Жуков, заведующий отделением клинической онкологии ФГУ ФНКЦ детской гематологии, онкологии и иммунологии
Н.В. Жуков, заведующий отделением клинической онкологии ФГУ ФНКЦ детской гематологии, онкологии и иммунологии
Для меня наиболее значимым событием 2010 г. явилось, наверное, заявление экспертов FDA о необходимости отзыва у бевацизумаба показания «метастатический рак молочной железы». С моей точки зрения это первый «звоночек» для фармацевтических гигантов, что эпоха крайне дорогихпрепаратов, которые лишь позиционируются, как целевые, а на самом деле используются эмпирически и из-за этого дают очень небольшой выигрыш, заканчивается. И судя по реакции фирмы производителя, предложившей провести новое большое подтверждающее исследование для поиска критериев отбора на лечения, этот «звоночек» услышан. Тем более это приятно, что мы говорили о вероятности подобного исхода еще 3 года назад на одном из Российских онкологических конгрессов.
Девиз: «мероприятия по совершенствованию оказания медицинской помощи онкологическим больным – приоритетный проект развития отечественного здравоохранения»
Национальная онкологическая программа – «Мероприятия по совершенствованию медицинской помощи онкологическим больным», рассчитанная до 2015 года, стартовала при тревожных показателях: второе место среди причин смертности занимают онкологические заболевания (13,2%); ежегодно выявляют 470 тыс. больных со злокачественными новообразованиями; неудовлетворительные показатели их активного выявления (12,9%).
Неотложными мерами по реализации программы явились:
Основными причинами для разработки и принятия вышеперечисленных нормативных актов послужили:
Выделение в рамках реализации приоритетного национального проекта «Здоровье» отдельного мероприятия, направленного на совершенствование оказания медицинской помощи онкологическим больным – Национальной онкологической программы, свидетельствует о значительном внимании Президента и Правительства Российской Федерации, Министерства здравоохранения и социального развития Российской Федерации, а также органов исполнительной власти субъектов Федерации к совершенствованию оказания медицинской помощи больным злокачественными новообразованиями.
В результате реализации Национальной онкологической программы онкологическая служба начала получать реальную финансовую поддержку из федерального и региональных бюджетов, позволяющую постепенно модернизировать и расширять оснащенность не только специализированных учреждений, оказывающих медицинскую помощь онкологическим больным, но и лечебно-профилактических учреждений общей лечебной сети.
Мероприятиями предусматривается:
В развитие приказа Минздравсоцразвития России от 3 декабря 2009 г. №944н «Об утверждении Порядка оказания медицинской помощи онкологическим больным» во всех субъектах Российской Федерации изданы приказы органов управления здравоохранением о порядке маршрутизации пациентов при подозрении или выявлении злокачественных новообразований, определены алгоритмы первичного диагностического обследования.
В соответствии с задачами, поставленными приказом Минздравсоцразвития России от 3 декабря 2009 г. №944н «Об утверждении Порядка оказания медицинской помощи онкологическим больным» перед первичными онкологическими кабинетами (отделениями) – они становятся проводниками совершенствования онкологической помощи. По данным паспортов онкологических диспансеров регионов в настоящее время в стране функционируют 2345 первичных онкологических кабинетов и отделений, при этом только 30% из них укомплектованы врачами-онкологами, в остальных работают врачи совместители, недостаточно обученные основам онкологии.
Учитывая трудности в регионах с укомплектование врачами-онкологами первичных онкологических кабинетов и отделений, Министерством предусмотрено возможность работы в кабинетах врачей-специалистов, прошедших подготовку по онкологии. Однако, органы исполнительной власти должны с полной ответственностью к подготовке и укомплектованию учреждений здравоохранения врачами – онкологами.
В стране ведется работа по формированию системы автоматизированного учета, регистрации и мониторинга онкологических заболеваний. На начало 2010 г. территориальные онкологические регистры на основе унифицированного единого программного обеспечения функционировали в 47 регионах. На сервере Министерства создана единая база онкологического регистра. В плане развития информационной составляющей Национальной онкологической программы в соответствии с планом-графиком Минздравсоцразвития России проведены организационно-методические занятия со специалистами, ответственными за ведение территориальных онкологических регистров 30 субъектов Российской Федерации. Онкологическим диспансерам регионов переданы электронные ключи доступа к информационной системе Минздравсоцразвития России. Работа по созданию Федерального онкологического регистра будет продолжена до полного включения всех регионов страны.
За 9 месяцев 2010 года для первичных онкологических кабинетов в территориях, включенных в программу 2009 года, было обучено 118 врачей по специальности «онкология» из 137 запланированных (т.е. 87,0%). Проведено обучение по основам онкологической дисциплины 773 врачей узких специальностей общей лечебной сети, в том числе: хирургов – 95, гинекологов – 111, урологов – 27, рентгенологов – 59, специалистов ультразвуковой диагностики – 48. Тем не менее, продолжает оставаться неудовлетворительной и вызывает тревогу проблема недостаточной укомплектованности специализированных лечебных учреждений медицинскими кадрами.
Разработаны, согласованы и переданы на утверждение в Минздравсоцразвития России стандарты оказания медицинской помощи больным со злокачественными новообразованиями по основным локализациям.
Научно-практическая конференция и Пленум Ассоциации онкологов России постановляют:
Руководителям департаментов, министерствам, главным специалистам неонкологического профиля, главным онкологам территорий, заведующим кафедрами онкологии, главным врачам онкологических диспансеров совершенствовать работу первичных онкологических кабинетов, улучшив укомплектованность их квалифицированными медицинскими кадрами, а также повысить уровень онкологической настороженности врачей общей практики.
Главным специалистам неонкологического профиля и главным врачам лечебно-профилактических учреждений обратить особое внимание на анализ причин запущенности онкологических заболеваний с принятием конкретных мер по каждому наблюдению.
Руководителям органов управления здравоохранением субъектов Российской Федерации, главным онкологам федеральных округов взять под особый контроль соблюдение сроков и качества реализации мероприятий по совершенствованию и развитию региональной онкологической службы.
Научно-исследовательским онкологическим институтам страны продолжить работу по совершенствованию федеральных алгоритмов диагностики и стандартов лечения больных злокачественными новообразованиями.
В системе непрерывной профессиональной подготовки медицинских кадров использовать современные информационные технологии, включая дистанционное обучение, телекоммуникации, компьютерные системы тестирования.
Активизировать работу по развитию телекоммуникационных технологий между регионами и федеральными онкологическими институтами.
Минздравсоцразвития России продолжить работу по созданию Федерального онкологического регистра взрослого и детского населения с интегрированием в информационно-аналитическую систему Министерства с учетом современных телекоммуникационных технологий.
Научно-исследовательским онкологическим институтам продолжить разработку и внедрение в клиническую практику новых медицинских технологий профилактики, диагностики, лечения и реабилитации больных злокачественными новообразованиями.
24 декабря 2010,
официальный интернет-сайт Минздравсоцразвития России
 С.А. Тюляндин, заместитель директора и заведующий отделением клинической фармакологии и иммунологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Председатель Российского общества клинической онкологии
С.А. Тюляндин, заместитель директора и заведующий отделением клинической фармакологии и иммунологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Председатель Российского общества клинической онкологии
Минздравсоцразвития делает основной упор в борьбе с онкологическими заболеваниями на раннюю диагностику и раннюю выявляемость. С этой целью производится активное переоснащение онкологических учреждений первичного звена, как материально-техническое, так и кадровое. Эти шаги, безусловно, очень важны, так как уровень оснащения большинства онкологических диспансеров в стране пока остается очень низким. Однако, на мой взгляд, проблема такого подхода в том, что недостаточно внимания уделяется тем людям, кто уже болен. На сегодня основное направление онкологической мысли в развитых странах – рассмотрение рака как системного процесса, развитие адъювантного лечения при солидных опухолях. Если целью реформ является снижение смертности от злокачественных опухолей, ее невозможно достигнуть без развития адъювантной химиотерапии после оперативных вмешательств при наиболее распространенных опухолях, к которым относятся рак молочной железы, легкого, яичника и толстой кишки. В России же все химиотерапевтическое лечение солидных опухолей относится к специализированной помощи, т.е. финансируется за счет ФОМС и региональных бюджетов. В настоящее время в России возникла ощутимая потребность в разработке стандартов и рекомендаций по лечению онкологических заболеваний с учетом современных научных достижений, и есть большое опасение, что средств, выделяемых сегодня на лечение больных солидными опухолями не будет достаточно для проведения им адекватной, современной и, главное, эффективной терапии.
Постановлением Правительства установлен порядок предоставления регионам субсидий из федерального бюджета на софинансирование мероприятий, направленных на совершенствование медицинской помощи больным с онкологическими заболеваниями. Общийобъем субсидий на 2011 год составит 5 млрд. 956 млн. 250 тыс. руб.
Для снижения смертности и инвалидности населения от онкологических заболеваний в 2009 году в рамках нацпроекта «Здоровье» начата реализация Национальной онкологической программы, которая предусматривает:
Выстраивая системный подход к организации онкологической помощи населению министерство совместно с ведущими специалистами в этой области ставит своей целью качественно преобразовать систему оказания первичной и специализированной, в том числе высокотехнологичной медицинской помощи; усилить роль первичного медико-санитарного звена для раннего выявления злокачественных новообразований; и повысить профессионализм медицинских работников.
Начиная с 2009 года в программные мероприятия включаются поэтапно регионы и федеральные учреждения, занимающиеся этой проблемой. Уже выделено на эти цели более 12 млрд. руб., с 2011 по 2013 предусмотрено более 21 млрд. руб.
В 2009 году в мероприятия были включены учреждения 11 регионов и 2 федеральных государственных учреждения 6 805 млн. руб.
В 2010 г. включены в программу 10 регионов и 3 федеральных учреждения. Направлено – 5 706,6 млн.руб.
В результате реализации Национальной онкологической программы онкологическая служба начала получать реальную финансовую поддержку из федерального и региональных бюджетов, позволяющую постепенно модернизировать и расширять оснащенность не только специализированных учреждений, оказывающих медицинскую помощь онкологическим больным, но и лечебно-профилактических учреждений общей лечебной сети.
Мероприятиями предусматривается:
Предоставление субсидии региону осуществляется на основании соглашения, в котором предусматриваются следующие условия:
В 2010 г. в реализацию программы включены 10 регионов (оснащение медицинским оборудованием 1 окружного и 9 региональных онкологических диспансеров, 5,8 млрд. рублей). За 2009 и 2010 учебные годы было направлено в интернатуру и ординатуру 472 специалиста, что позволит снизить дефицит врачей-онкологов почти на 10%.
В стране ведется работа по формированию системы автоматизированного учета, регистрации и мониторинга онкологических заболеваний (Национальный онкологический регистр). На начало 2010 г. территориальные онкологические регистры на основе унифицированного единого программного обеспечения функционировали в 47 регионах. На сервере Министерства создана единая база онкологического регистра. В плане развития информационной составляющей Национальной онкологической программы в соответствии с планом-графиком Минздравсоцразвития России проведены организационно-методические занятия со специалистами, ответственными за ведение территориальных онкологических регистров 30 субъектов Российской Федерации. Онкологическим диспансерам регионов переданы электронные ключи доступа к информационной системе Минздравсоцразвития России. Работа по созданию Федерального онкологического регистра будет продолжена до полного включения всех регионов страны.
За 9 месяцев 2010 года для первичных онкологических кабинетов в территориях, включенных в программу 2009 года, было обучено 118 врачей по специальности «онкология» из 137 запланированных (т.е. 87,0%). Проведено обучение по основам онкологической дисциплины 773 врачей узких специальностей общей лечебной сети, в том числе: хирургов – 95, гинекологов – 111, урологов – 27, рентгенологов – 59, специалистов ультразвуковой диагностики – 48.
Отмечается значительный прирост, более чем на 22% числа проведенных обследований в первичных онкологических кабинетах, что свидетельствует об увеличении обращаемости в первичные онкологические кабинеты и, косвенно, о повышении «онконастороженности» врачей первичного звена здравоохранения и эффективности мер по повышению информированности граждан.
Более 11% пациентов проходит через региональные и окружные онкологические диспансеры, что свидетельствует о совершенствовании организации маршрутизации пациентов.
В ходе реализации мероприятий увеличилось число диагностических исследований. Растет частота исследований на онкологические маркеры. Все чаще стали использоваться радиоизотопные методы исследования, которые до настоящего времени не получали широкого применения.
Впервые наблюдается замедление темпов роста показателя смертности от онкологических заболеваний в Российской Федерации, что в целом говорит об эффективности всего комплекса проводимых мероприятий, включая профилактику, своевременность выявления и повышение доступности к современным методам лечения.
 12 января 2011 г.,
12 января 2011 г.,
официальный интернет-сайт
Минздравсоцразвития России
В начале февраля 2011 года была создана Торакальная рабочая группа Российского общества клинической онкологии. Группу возглавила заведующая отделением химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, профессор Горбунова Вера Андреевна.
В Чешской республике сложилась патовая ситуация: врачи больниц, в основном расположенных в провинции, в массовом порядке подали заявления об увольнении с марта этого года.
Главным требованием врачей является увеличение зарплат в два-три раза по сравнению с нынешними окладами. В ответ на эту акцию министр здравоохранения Леош Хегер заявил, что рассматривает возможность объявления в этих регионах режима чрезвычайной ситуации, что подразумевает мобилизацию врачей, даже тех, которые на данный момент официально не работают.

В некоторых регионах страны о своем желании уволиться заявили рекордное количество врачей. Например, в крае Высочина хотят покинуть работу 59 процентов врачей, а в столице края Йиглаве аж 72 процента. Тревожная ситуация также сложилась в Северной Моравии, а также в городах Градец Кралове и Брно. В общей сложности в стране заявления об уходе подали 3800 врачей, при том, что общее число врачей в Чехии составляет 18 тысяч.
Как считают эксперты, к кризису привели проблемы в устройстве системы медицинского образования в республике и дисбаланс в финансировании.
Слишком долго учиться
Система медицинского образования в Чехии устроена довольно консервативно. Для того чтобы получить возможность работать в больнице, студент должен шесть лет проучиться на медицинском факультете. Но получение диплома о высшем образовании не означает, что выпускник вуза может открыть частную практику (которая и приносит более-менее стабильный доход).
Для того чтобы получить возможность работать самостоятельно, молодой врач должен отработать в общей сложности шесть лет в больницах с государственной аккредитацией на образование врачей (с нюансами это аналог американской интернатуры), проходя ротацию во всех отделениях больницы от скорой помощи до геронтологии. По окончании каждого курса практики врач получает удостоверение, и только наличие удостоверений о том, что все необходимые стажировки пройдены, дают право на открытие частной практики или дальнейшую работу по профилю.
В общей сложности процесс занимает около шести лет и все это время врачи привязаны к больницам фактически на кабальных условиях. Средняя зарплата молодого врача составляет 15 000 крон (приблизительно 700 долларов) – прожить на это практически невозможно. Если брать ночные дежурства и работу в праздники, можно заработать примерно еще столько же, но это работа на износ. Уйти из больницы или сократить время стажировки нельзя.
Деньги на медицину есть
Нельзя сказать, что в Чешской республике существует проблема с финансированием медицины. На развитие медицины страховые компании, государство и региональные власти потратили – в 2005 году 218 миллиардов крон, в 2006 году – 226 миллиардов крон, в 2007 году – 241 миллиард крон, в 2008 году – 262 миллиарда крон, и расходы продолжают расти.
Проблема в том, что деньги вкладываются не в зарплатный фонд, а в реконструкцию больниц и приобретение оборудования. Важную роль играет тот факт, что распоряжаются бюджетами на медицину региональные власти. А поскольку забота о здоровье граждан – хороший повод чтобы набрать политические очки перед выборами, то региональные власти предпочитают тратить деньги не на такое банальное предприятие как зарплаты для врачей в больницах, а на закупку редкого оборудования в каком-нибудь захолустье или открытие отделения онкологии в больнице, при том, что аналогичное существует в десяти километрах.
Восстание врачей
В Чехии существует две организации, которые занимаются соблюдениями прав врачей. Первая «Чешская палата врачей», в которой состоят все врачи республики и в обязательном порядке отчисляют в нее взносы. В случае проблем Палата берет на себя функции третейского судьи или представителя интересов корпорации перед государством. Палата связана с государственными структурами множеством обязательств, так что не может отстаивать интересы врачей радикальными способами. Другая организация – «Врачебный профсоюзный клуб», участие в ней менее формально, а ее действия более радикальны. Характерно, что нынешний председатель Палаты Милан Кубек в прошлом был руководителем Врачебного профсоюзного клуба.
В сентябре прошлого года Врачебный профсоюзный клуб начал акцию за повышение зарплат врачей, работающих в больницах. Для начала они наняли юристов и провели детальный анализ законодательства. Выяснилось, что по чешским законам врачи не могут объявить забастовку, так как эта профессия считается жизненно важной для функционирования общества. Однако юристы предложили другой путь: врачи могли подать заявление об увольнении. С учетом того, что заявление по закону должно быть подано за три месяца до увольнения, а врачам, оказавшимся без работы (даже по личной инициативе), гарантировано пособие в 60 процентов от зарплаты, врачи не подвергались особому риску. Таким образом Клуб пришел к выводу, что нужно предложить врачам уволиться, для того чтобы потребовать повышение зарплаты.
Для проведения кампании Клуб нанял профессиональных пиарщиков – компанию «Ewing PR». Бюджет кампании составил 3,5 млн. крон. Кампания получила название «Спасибо, мы уходим».
Для того чтобы начать агитационную компанию, Клуб купил машину «Скорой помощи» семидесятых годов и раскрасил ее в черно-белый цвет. На белой стороне машины было написано «Наш исход…», на черной стороне – «Ваша смерть». Машина разъезжала по всей Чехии. Клуб выбрал четырех врачей, которые представляли кампанию. Главным лицом кампании стал врач Павел Вавра, который ездил на этой машине, на улицах измерял людям давление, проводил первичные консультации, и объяснял смысл кампании. То же самое делали и его соратники.
Кроме того, Клуб рассылал врачам предложение уволиться, где честно излагал все риски этого шага. Про риски следует сказать отдельно. Кроме пособия по безработице, у чешских врачей есть очень неплохой шанс найти работу за границей. В немецких и австрийских медицинских изданиях уже несколько лет публикуются объявления о приеме на работу чешских врачей. Причем немцы, в отличие от чехов, не требуют прохождения полного курса практики и готовы взять выпускников вузов. Аналогичную заинтересованность проявляют шведы и англичане. Так что у чешских врачей есть некоторые рычаги давления на госструктуры.
Чем сердце успокоится
Чехия замерла в преддверии кризиса. Но уже сейчас видно, что государство готово идти на уступки. Премьер-министр Чешской республики (а его политический вес, в силу того что Чехия – парламентская республика, существенно выше чем у президента) на встрече с председателем Чешской палаты врачей пообещал потратить деньги, сэкономленные при реформе здравоохранения, на зарплаты. Однако на данный момент непонятно, насколько доходы от реформы смогут удовлетворить требования врачей.
Женя Снежкина (Прага)
Источник: denik.cz
Газета Российского общества клинической онкологии – Выпуск 04 • 2011 – Номер подготовлен: И. Тимофеев, Д. Стефанов – Издается 2 раза в месяц. Распространяется бесплатно среди членов общества. Адрес редакции: 119021, Москва, ул. Тимура Фрунзе, 16/3, офис 21-22, тел. (499) 245 50 78, e-mail:
При перепечатке материалов необходимо получить разрешение редакции.