27.05.2013
Несколько дней осталось до открытия очередного конгресса Американского общества клинической онкологии (ASCO), который пройдет в Чикаго с 31 мая по 4 июня 2013 года. Одним из важных событий конгресса станет выступление Джедда Волчока, который представит 2 июня основные результаты крайне интригующего клинического исследования 1-й фазы по использованию иммунотерапии при лечении распространенной меланомы. Абстракт исследования, посвященного оценке безопасности и клинической активности комбинации Ниволумаба с Ипилимумабом, уже сейчас доступен на сайте конгресса.
Лишь немногие препараты показали свою эффективность уже на этапе I фазы клинических испытаний, основной целью которых всегда считалась оценка переносимости (но не эффективности). Комбинированная иммунотерапия Ниволумабом и Ипилимумабом показала свою активность уже в 1-й фазе исследования. Со слов доктора Волчока, на февраль 2013 г. в исследование вошли 86 человек. Ответ опухоли на комбинированную иммунотерапию наблюдался у 90% из 52 пациентов, данные о которых уже сейчас поддаются оценке. Необходимо учитывать то, что все пациенты имели нерезектабельную меланому III или IV стадии и до включения в исследование уже получили несколько различных схем лечения (вне рамок данного исследования подобные пациенты подлежали бы лишь симптоматической терапии).
Препарат Ниволумаб, разработанный компанией Бристол-Майерс Сквибб, представляет собой моноклональное антитело, чье действие направлено против белка PD-1 экспрессированного на T-лимфоцитах. Действие препарата Ипилимумаба, разработанного той же компанией, направлено против белка CTLA-4, который также экспрессированн на T-лимфоцитах (рис. 1). Объединенный механизм действия этих препаратов на иммунную систему позволяет достичь большего ответа со стороны опухоли, чем если бы они использовались по отдельности.
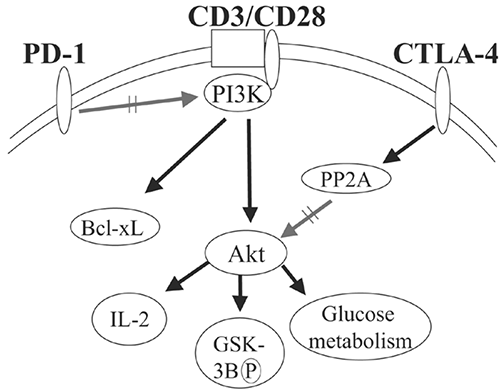
Рисунок 1. Модель CTLA-4- и PD-1-опосредованного ингибирования Т-лимфоцитов.
(Parry RV et al. Mol. Cell. Biol. 2005; 25:9543-9553)
Эскалация доз ипилимумаба до 3 мг/кг в день и ниволумаба до 1 мг/кг в день позволила добиться объективного опухолевого ответа у 53% из 17 пациентов. При этом у 7 пациентов (41%) наблюдалась редукция опухолевой массы более 80% к 12 недели терапии (таб.1). Частота полных ответов составила 17%. «Результаты лечения действительно поразительны», – отмечает президент ASCO, доктор медицины Сандра Свейн. «Такого рода ответа на иммунотерапию ранее не наблюдалось», – добавляет она.
Таблица 1. Частота ответов при комбинированной терапии иплимумабом и ниволумабом
| Когорта | Ипилимумаб (мг/кг) + ниволумаб (мг/кг) |
Кол-во пациентов | ПО | ЧО | ЧОО (%) (95% ДИ) |
Уменьшение в размерах опухоли > 80% к 12 неделе (%) |
|---|---|---|---|---|---|---|
| 1 | 3 + 0,3 | 14 | 1 | 2 | 21 (5-51) | 4/14 (29) |
| 2 | 3 + 1 | 17 | 3 | 5 | 47 (23-72) | 7/17 (41) |
| 3 | 3 + 3 | 6 | 0 | 3 | 50 (12-88) | 0/6 (0) |
ПО – полный ответ, ЧО – частичный ответ, ЧОО – частота объективных ответов.
Нежелательные явления 3-4 степени на фоне комбинированной иммунотерапии наблюдались у 53% пациентов, большей частью без клинических симптомов, только в виде повышений концентраций липазы (11%), печеночных ферментов – АЛТ (11%) и АСТ (13%). Максимальная токсическая доза была достигнута в 3-й когорте у 59% пациентов и проявлялась развитием увеитов/хориоидитов, колитов и обратимых изменений в лабораторных анализах. Смертей, связанных с лечением, в исследовании зарегистрировано не было.
В другом клиническом исследовании 1-й фазы, результаты которого будут доложены 3 июня, новый препарат MPDL3280A в виде монотерапии назначался пациентам с местно-распространенными и метастатическими формами солидных злокачественных новообразований. MPDL3280A является моноклональным антителом к рецептору белка PD-1, разработанного компанией «Генентех». В ранее проведенных исследованиях было показано, что высокая экспрессия рецептора белка PD1 на опухолевых клетках почечно-клеточного рака связана с более высокой смертностью пациентов.
Объективный ответ со стороны опухоли наблюдался у 29 (21%) из 140 пациентов, включенных в исследование. MPDL3280A был наиболее активен при меланоме, немелкоклеточном раке легкого и почечноклеточном раке. Незначительный ответ наблюдался при злокачественных новообразованиях головы и шеи, желудка, ободочной кишки и мочевого пузыря.
26 из 29 пациентов ответили на терапию MPDL3280A в сроки от 3 до 15 месяцев от начала лечения. 24-недельная безрецидивная выживаемость составила 44%. Частота объективных ответов на терапию была выше у тех пациентов, опухоли которых экспрессировали PD-L1, по сравнению с опухолями пациентов, не экспрессирующих этот рецептор (36% против 13%).
При эскалации доз до максимальных 20 мг/кг в сутки минимальная токсическая доза препарата достигнута не была. У 43% пациентов наблюдались нежелательные явления 3-4 степени во время терапии MPDL3280A. Со слов исследователей, только 13% из них были обусловлены действием препарата. В основном, нежелательные явления были опосредованы самим заболеванием или возникали по другим причинам.
Подробнее о результатах этих исследований можно будет узнать на конференции Российского общества клинической онкологии «ЛУЧШЕЕ ПО МАТЕРИАЛАМ СИМПОЗИУМОВ И КОНГРЕССОВ 2013».
Новость подготовил: Р.Т. Абдуллаев, к.м.н., ассистент кафедры онкологии и лучевой терапии педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава России.
Источники: